요약목적:비록 fisetin의 다양한 생리활성이 보고되었음에도 불구하고, fisetin의 미용기능식품 소재로서의 가능성에 대한 연구는 미비한 실정이다. 그러므로, 본 연구에서는 fisetin의 항산화 활성 및 3T3-L1 세포에서 fisetin의 항비만 활성을 평가하고, 더 나아가 미용기능식품 소재로서 fisetin의 가능성에 대해 고찰하였다.
방법:Fisetin의 항산화 활성은 ABTS 라디칼 소거능을 통해 평가하였다. 3T3-L1 세포에서 fisetin의 세포독성은 EZ-cytox assay를 이용해 분석하였으며, fisetin의 지방축적 억제활성은 triglyceride 함량 분석을 통해 평가하였다. 또한 fisetin이 지방세포 분화전기(Day -2~0), 분화초기(Day 0~2), 분화중기(Day 2~4), 분화후기(Day 4~6)와 같은 3T3-L1 adipogenesis의 다양한 단계 중 어느 단계에서 억제 효과를 가지는지 ORO 염색법을 통해 알아보았다. 3T3-L1 세포에서 전사인자들의 mRNA 발현 수준은 RT-PCR을 통해 분석하였다.
결과:Fisetin은 항산화 물질로 잘 알려진 비타민C (L-ascorbic acid)보다 강한 ABTS 라디칼 소거활성을 나타내었다. 또한 fisetin을 24 h 동안 처리하였을 때, 200 μM 이하의 농도에서 3T3-L1 세포생존율에 영향을 미치지 않았다. 따라서 fisetin을 100 μM 이하의 농도로 다음 실험에 이용하였다. 3T3-L1 세포에서 triglyceride 함량은 농도 의존적으로 감소시켰다. Fisetin이 adipogenesis 어떠한 단계에서 지방축적 억제활성을 나타내는지 알아보았을 때 분화전기(Day -2~0), 분화초기(Day 0~2), 그리고 분화중기(Day 2~4)에 가장 높은 억제활성을 나타내었다. 또한 fisetin에 의한 adipogenesis의 억제는 C/EBPβ, leptin, 그리고 adiponectin의 감소된 mRNA 발현수준에 의한 것으로 사료된다.
AbstractPurpose:Although several physiological properties of fisetin have been reported, the potential of fisetin as a nutri-cosmetics material has been not considered. Therefore, anti-oxidant and anti-adipogenic effects in 3T3-L1 cells of fisetin were evaluated and its potential as a nutri-cosmetic ingredient was discussed.
Methods:To test anti-oxidant activity of fisetin, ABTS radical scavenging assay was used and the cytotoxicity of fisetin in 3T3-L1 preadipocytes was evaluated by EZ-cytox assay. The inhibitory effect of fisetin against 3T3-L1 adipogenesis was evaluated in various stage of adipogenesis such as pre-adipogenic (Day -2~0), early (Day 0~2), intermediate (Day 2~4), and terminal stage (Day 4~6) by oil red o (ORO) staining. The mRNA expression levels of transcriptional factors were performed by RT-PCR analysis.
Results:We observed that the scavenging activity of fisetin against ABTS radicals was stronger than that of ascorbic acid, a well-known soluble anti-oxidant. Fisetin treatment resulted in the decreased triglyceride content of 3T3-L1 cells in a dose-dependent manner. Lipid accumulation of 3T3-L1 adipocytes was significantly inhibited by fisetin treatment by 54.61%, 61.74%, 56.82%, and 26.67%, respectively when compared to adipocytes control. The anti-adipogenic effect of fisetin was strongly limited in the pre-adipogenic, early, and intermediate stages of 3T3-L1 adipogenesis. In addition, the fisetin treatment down-regulated mRNA expression levels of C/EBPβ, leptin, and adiponectin in mature 3T3-L1 adipocytes.
中文摘要目的: 虽然漆黄素(fisetin)有很多种生理活性,但是现阶段作为美容功能性材料可行性的研究很少。因此通过评价漆黄素的抗氧化活性以及在3T3-L1细胞中漆黄素的抗肥胖性,进一步调查美容功能性食品材料的可行性。
方法: 漆黄素的抗氧化活性通过消除ABTS激进评价。在3T3-L1细胞中漆黄素的细胞毒性利用EZ-cytox assay分析,漆黄素的抑制脂肪堆积是通过测量甘油三酸酯的含量而评价。3T3-L1细胞的脂肪形成阶段分为4阶段:分化前期(Day -2~0)、分化初期(Day 0~2)、分化中期(Day 2~4)、分化后期(Day 4~6)。通过利用ORO染色法调查漆黄素的抑制效果出现在哪个脂肪形成 阶段。3T3-L1细胞中利用RT-PCR法分析转录因子的mRNA表达。
Introduction비만(Obesity)은 생체 내 불균형적인 에너지의 축적과 소비로 인해 일어나는 대사성 질환의 하나로 개인의 정신적, 육체적, 그리고 환경적 요인의 변화 등으로 인한 인체의 항상성 변화에 의해 나타난다(Ji et al., 2012). 비만은 당뇨, 심혈관질환, 고혈압, 그리고 고지혈증 등과 같은 대사성 질환을 유발할 뿐만 아니라 각종 암의 발생빈도를 증가시켜 수명을 단축시킨다고 알려져 있다(Choi et al., 2012). 비만은 전지방세포의 지방세포 분화과정인 adipogenesis에 의해 세포내 중성지방(triglyceride)의 축적 등에 의해 발생되는 것으로 보고되어지고 있으며, 비만에 있어 adipogenesis를 조절하는 것은 비만 예방 및 치료를 위한 효과적인 방법으로 제시되고 있다(Park et al., 2013).
Adipogenesis는 전지방세포가 지방세포로 분화되는 과정을 말하며, 지방세포 분화 초기에 발현되는 전사인자인 CCAAT/enhancer-binding protein β(C/EBPβ)와 C/EBPδ가 peroxisome proliferator-activated receptor γ(PPARγ)와 C/EBPα의 발현을 유도하여 fatty acid synthase (FAS), fatty acid binding protein 2 (aP2), leptin, 그리고 adiponectin과 같은 지방세포내 특이적 유전자의 발현을 통해 중성지방구의 수 및 크기를 증가시킨다(Tzeng & Liu, 2013). 이전의 연구에서는 녹차의 주요한 카테킨 성분 중 하나인 epigallocatechin-3-gallate (EGCG)와 글루코사민 유도체인 glucosamine 6-phosphate가 adipogenesis 과정에서 중요한 역할을 하는 C/EBPα, PPARγ, FAS, 그리고 Lipoprotein lipase (LPL)과 같은 전사인자 및 지방세포 특이적 유전자들의 mRNA 발현을 억제함으로서 adipogenesis 억제를 통해 항비만 활성을 가진다는 것이 보고되었다(Kim & Jang, 2014). 또한 알칼로이드로 알려진 meridianin C가 C/EBPα, PPARγ, leptin, 그리고 adiponectin과 같은 전사인자들을 조절함으로써 adipogenesis를 억제하여 항비만 활성을 가진다는 결과가 보고되었다(Park et al ., 2014). 이상의 보고는 adipogenesis 억제에 있어 전사인자의 발현을 조절하는 것은 중요한 항비만 분자생물학적 전략임을 의미한다.
우리 몸에서는 에너지 생산을 위한 산화·환원 과정 중 상당량의 활성 산소들이 생성된다. 정상적인 상태에서 생체 내 제거 기작에 의해 활성 산소들이 대부분 소거되지만, 과도하게 생성된 활성 산소는 체내 항산화 방어 시스템의 균형을 깨트리고 비만 및 피부질환을 비롯하여 각종 질병의 원인이 된다(Shon & Kim, 2014). 특히 비만에 의해 증가된 지방세포는 지질과산화물의 형성을 촉진하여 체내 항산화 시스템의 불균형을 야기하여 산화적 스트레스를 유발한다고 알려져 있다(Kim et al ., 2014). 따라서 항산화 방어 시스템을 향상시키는 것은 활성 산소로부터 비만 및 피부질환 등 각종 질환의 발생을 예방하거나 지연시키는데 중요한 역할을 한다. 최근 적은 부작용과 안전성이 확보된 식품소재 및 천연물 소재를 활용하여 산화적 스트레스 및 adipogenesis 억제를 통해 비만을 예방하고자 하는 다양한 노력들이 시도되고 있다(Park et al ., 2015).
미용기능식품은 약용 화장품과 건강기능식품의 중간 형태로 미용의 목적을 가진 보조식품으로 정의할 수 있다(Anuntiato & da Rocha Filho, 2012). 사과, 감, 양파, 포도, 그리고 오이 등과 같은 과일이나 채소에 많이 함유된 성분인 fisetin은 플라보노이드 중 플라보놀 그룹에 속하며, 생물 체내에서 세포신호전달, 유전자 및 단백질의 발현, 그리고 세포분화 등에 관여한다(Kim et al ., 2012). Fisetin에 대한 연구로는 항염증(Seo & Jeong, 2015), 그리고 고암모니아혈증 완화(Subramanian et al ., 2015) 등의 효과가 보고되었지만, adipogenesis 억제에 있어 분자학적 메커니즘은 아직 명확하게 밝혀지지 않았다. 따라서 본 연구에서는 ABTS 라디칼 소거 활성을 통해 fisetin의 항산화 활성을 평가하였다. 또한 3T3-L1 세포에서 fisetin이 지방세포분화 초기단계에 발현되는 전사인자인 C/EBPβ 에너지 섭취 및 소비에 관여하는 leptin 호르몬, 그리고 포도당 대사 및 지방산 산화에 있어 중요한 역할을 하는 adiponectin과 같은 adipogenesis 특이적 유전자들의 발현에 어떠한 영향을 미치는지 알아보았다. 더 나아가 fisetin이 adipogenesis의 분화전기, 초기, 중기, 그리고 후기 단계 중 어떠한 단계에 작용하여 adipogenesis를 억제하는지 평가하였으며, 미용기능식품 소재로서의 가능성에 대해 고찰하였다.
Methods1. 실험재료본 실험에 사용된 fisetin, Oil Red O (ORO), 3-isobutyl-1-methylxanthine (IBMX), insulin, dexamethasone (DEX), 2,2’-azinobis-3-ethyl-benzothiazoline-6-sulfonic acid (ABTS), potassium persulfate, 그리고 chloroform는 Sigma-Aldrich Co. (St. Louis, MO, USA)에서 구입하여 사용하였으며, Dulbecco’s modified Eagle’s medium (DMEM), penicillin-streptomycin, bovine calf serum (BCS) 그리고 RNase-free water는 WELGENE Inc. (Daegu, Korea)에서 구입하여 사용하였다. Fetal bovine serum (FBS)은 Gibco BRL. (Carlsbad, CA, USA)에서 구입하였으며, EZ-Cytox cell viability assay kit은 Daeil Labservice (Seoul, Korea)에서 구입하여 사용하였다. EnzyChrom™ triglyceride assay kit는 Bio Assay Systems (Hayward, CA ,USA)에서 구입하여 사용하였다. Formaldehyde는 Bio Basic Inc. (Markham, ON, Canada), TRIzolⓇ은 Life Technologies (Carlsbad, CA, USA)에서 구입하였으며, AccuPowerⓇ CycleScript RT PreMix는 Bioneer (Daejeon, Korea)에서 구입하여 사용하였다. 3T3-L1 전지방세포는 한국세포주은행(Seoul, Korea)에서 분양받아 사용하였다.
2. Fisetin의 ABTS 라디칼 소거활성 평가Fisetin의 항산화 활성은 Re 등의 방법을 일부 변형한 ABTS 라디칼 소거활성을 이용하여 평가하였다(Re et al ., 1999). 7 mM ABTS와 2.45 mM potassium persulfate를 증류수에 녹인 다음 12 h 차광하여 ABTS 라디칼을 생성하였다. 이 반응액을 증류수를 이용하여 415 nm의 흡광도에서 1.5±0.02로 맞추어 희석하였다. ABTS 반응액 95 μL에 농도별 시료 5 μL를 가하여 실온에서 10 min 동안 반응시킨 후, 415 nm에서 흡광도를 측정한 값을 아래의 식에 따라 계산하여 산출하였다. 양성대조군으로는 수용성 항산화제로 잘 알려진 L-ascorbic acid (비타민 C)를 사용하였다.
ODcontrol : 시료가 들어가지 않은 경우(대조군) 흡광도
ODsample : 시료가 들어간 경우 흡광도
3. 3T3-L1 세포에서 fisetin의 세포독성 평가Fisetin의 세포독성은 EZ-cytox cell viability assay kit을 이용하여 평가하였다. fisetin은 3T3-L1 전지방세포가 100% confluent 된 상태에서 10, 20, 40, 60, 80, 100, 그리고 200 μM의 농도로 24 h 동안 처리하였다. 이후 fisetin이 포함된 배지에 5%의 EZ-cytox cell viability kit을 처리한 후, 37℃, 그리고 CO2 incubator에서 1 h 동안 추가로 배양하였다. 배양 후 96-well plate에 배지를 100 μL/well씩 옮겨 microplate reader (Molecular Devices, Sunnyvale, CA, USA)를 사용하여 450 nm에서 흡광도를 측정하였다. fisetin을 처리하지 않은 3T3-L1 전지방세포를 대조군으로 하여 세포생존율(% of Control)을 계산하였다.
4. 3T3-L1 세포 배양 및 지방세포 분화3T3-L1 전지방세포는 DMEM 배지에 10% BCS와 1% penicillin-streptomycin을 첨가한 후 37℃, 5% CO2 환경에서 배양되었다. 3T3-L1 세포의 지방세포 분화와 fisetin의 처리는 Figure 1에 나타내었다. 3T3-L1 전지방세포가 confluent된 상태를 Day -2라고 표기하고, 분화유도 배지(Differentiation medium; DM)를 이용하여 지방세포 분화를 유도한 날을 Day 0라고 표시하였다. 분화유도 배지는 10% FBS와 1% penicillin-streptomycin이 첨가된 DMEM 배지에 500 μM의 IBMX, 5.2 μM의 DEX, 그리고 167 nM의 insulin을 포함하여 Day 0부터 Day 2까지 48 h 동안 처리하였으며, 분화유도 후 배지(Post-differentiation medium; Post-DM)는 10% FBS와 1% penicillin-streptomycin이 첨가된 DMEM 배지에 167 nM의 insulin만을 추가하여 Day 2에서 Day 4까지 사용하였다. 이후 DMEM 배지에 10% FBS와 1% penicillin-streptomycin을 첨가한 후 Day 4에서 Day 6까지 사용하였으며 Day 6에 지방세포 분화를 종료하였다.
5. 3T3-L1 세포의 triglyceride 함량 측정3T3-L1 세포의 triglyceride 함량은 triglyceride assay kit를 사용하여 분석하였다. 3T3-L1의 지방세포 분화는 위의 방법과 동일하게 이루어졌으며, Day 6에 지방세포를 PBS로 세척한 후 lysis buffer (5% triton-X 100 in PBS)를 이용하여 세포를 수확하였다. 이후 17,000 rpm으로 5 min 동안 원심분리한 후 상등액을 수거하였으며 assay buffer, enzyme mix, lipase, ATP, 그리고 dye reagent와 혼합하여 30 min 동안 상온에서 반응시킨 다음 570 nm에서 흡광도를 측정하였다. Triglyceride 함량은 μM/L로 표시하였다.
6. 분화 기간별 fisetin 처리에 따른 adipogenesis 억제활성 평가3T3-L1 세포에서 fisetin이 adipogenesis를 억제하는지 확인하기 위하여, fisetin을 분화이전(A), 분화초기(B), 분화중기(C), 그리고 분화후기(D)로 나누어 100 μM의 농도로 fisetin을 처리한 후 세포내 지방축적량을 ORO 염색법을 통해 분석하였다. ORO 염색은 Day 6에 실시하였으며, 분화가 완료된 3T3-L1 지방세포를 0.5 mL의 PBS를 넣어 세척한 후 3.7%(v/v)의 formaldehyde로 30 min 동안 실온에서 고정시켰다. 이후 흐르는 물에 3번 씻어 formaldehyde를 제거한 후 3 mg/mL의 ORO를 가하여 실온에서 15 min 동안 염색하였다. 증류수를 이용하여 ORO가 염색된 세포를 세척하고 남아있는 수분을 완전히 제거하였다. 그 후, 300 μL의 DMSO을 가하여 세포내 ORO를 녹여 100 μL/well씩 96-well plate에 옮겨 microplate reader를 이용하여 510 nm에서 흡광도를 측정하였다. Fisetin을 처리하지 않고 분화를 유도한 지방세포를 대조군으로 하여 지방축적량(% of control)을 계산하였다.
7. Reverse transcription-PCR (RT-PCR) 분석을 통한 유전자 발현 분석3T3-L1 세포는 10, 25, 50, 그리고 100 μM의 fisetin에 Day -2에서 Day 6까지 처리되었다. Day 6에 TRIzolⓇ을 이용하여 total RNA를 추출하였다. 추출된 total RNA에 100 μL의 chloroform을 넣고 15 s 동안 흔들어 잘 혼합해 준 후, 3 min 동안 상온에 정치한 뒤 20 min 동안 4℃ 온도에서 17,000 rpm으로 원심분리하여 상등액을 분리하였다. 얻은 상등액에 250 μL의 isopropanol를 넣고 잘 섞어준 후 10 min 동안 상온에 한번 더 정치한 다음 17,000 rpm, 4℃의 온도에서 15 min 동안 원심분리하여 mRNA를 분리하였다. 분리된 mRNA는 RNase-free water에 녹이고 정량한 뒤 bioneer을 이용하여 cDNA를 합성하였다. 합성된 cDNA는 thermal cycler (T100, Bio-Rad, USA)를 이용하여 PCR을 수행한 후 1.5% (w/v) 아가로즈 젤에 전기영동하여 mRNA 유전자 발현수준을 분석하였다. 본 실험에 사용된 C/EBPβ, leptin, 그리고 adiponectin의 primer sequences는 Table 1에 나타내었다.
Results and Discussion1. Fisetin의 ABTS 라디칼 소거활성L-ascorbic acid와 fisetin의 ABTS 라디칼 소거활성은 Figure 2A, 2B에 각각 나타내었다. ABTS의 라디칼을 50% 저해하는 농도인 fisetin의 IC50는 1.35 μg/mL로 나타났으며, 이는 항산화 비타민으로 잘 알려진 비타민C, L-ascorbic acid의 IC50 (2.91±0.04 μg/mL)와 비교하였을 때 더 강한 ABTS 라디칼 소거활성을 나타냈다. 이전 연구에서는 fisetin이 DPPH 라디칼 소거능 활성을 증가시키며, streptozotocin에 의해 유도된 당뇨 rat과 비교하였을 때 fisetin의 섭취는 당뇨 유도된 rat에서 TBARS 수치를 감소시켜 산화적 스트레스를 예방한다는 연구가 보고되었다 (Echeverry et al ., 2015; Prasath & Subramanian, 2013). 따라서 flavonoid 일종인 fisetin은 ABTS 라디칼 소거활성을 통해 체내 산화적 스트레스와 이에 기인하는 피부의 노화 예방에 기여할 수 있을 것으로 기대된다.
2. 3T3-L1 세포에서 fisetin의 세포독성 평가Fisetin이 3T3-L1 전지방세포에서 독성을 나타내는지 알아보기 위해 EZ-cytox assay를 통해 세포생존율을 평가하였다. Fisetin을 10, 20, 40, 60, 80, 100, 그리고 200 μM의 농도로 3T3-L1 전지방세포에 24 h 동안 처리한 결과, 각각 100.63%, 103.19%, 101.00%, 97.93%, 101.82%, 그리고 100.73%의 세포생존율을 나타냈으며 유의적인 차이는 관찰되지 않았다(Figure 3). 따라서 이후 실험에서는 세포 생존율에 영향을 미치지 않는 범위 중 100 μM 이하의 농도에서 실험을 진행하였다.
3. 3T3-L1 세포의 triglyceride 함량 측정3T3-L1 전지방세포를 Figure 1의 실험방법과 동일하게 분화시키고 fisetin을 Day -2에서 Day 6까지 처리한 후 Day 6에 triglyceride 함량을 측정하였다. 그 결과 분화시키지 않은 전지방세포의 triglyceride 함량과 비교하였을 때 아무것도 처리하지 않고 분화만 시킨 지방세포에서 다량의 triglyceride가 생성되었다(Figure 4). 3T3-L1 cells에 1, 10, 25, 50, 그리고 100 μM fisetin 처리는 대조군과 비교하였을 때 농도 의존적으로 triglyceride 함량을 감소시켰다. 이전 연구에서는 10, 25, 50, 그리고 75 μg/mL로 처리된 삼백초 추출물이 3T3-L1 지방세포에 작용하여 농도의존적으로 triglyceride 함량을 감소시켰으며(Shin et al ., 2012), 동과 분획물을 50 μg/mL의 농도로 처리한 후 세포내 triglyceride의 함량을 측정 하였을 때, 대조군과 비교하여 유의적으로 감소시켰다고 보고되었다(You & Jun, 2012). 따라서, 이 연구결과는 fisetin이 3T3-L1 adipogenesis 과정 중 생성되는 triglyceride 축적을 억제시켜 비만을 예방하는데 도움을 줄 것이라고 보여진다.
4. 분화 기간별 fisetin 처리에 따른 adipogenesis 억제활성3T3-L1 지방세포 분화모델을 이용하여 fisetin이 3T3-L1 adipogenesis를 억제하는지 확인하고자 하였다. 3T3-L1 전지방세포를 지방세포로 분화시키면서 fisetin을 분화이전(A), 분화초기(B), 분화중기(C), 그리고 분화후기(D)로 나누어 fisetin을 100 μM의 농도로 처리한 후, Day 6에 ORO 염색법을 통해 평가하였다. 그 결과, 분화되지 않은 전지방세포에서는 지방구 축적이 거의 이루어지지 않았으며, fisetin을 처리하지 않고 분화를 시킨 지방세포 대조군은 다량의 지방구가 형성되었다. Fisetin을 100 μM 농도로 분화이전(A), 분화초기(B), 분화중기(C), 그리고 분화후기(D)에 처리하였을 때 지방축적률은 지방세포 대조군과 비교하여 분화전기, 초기, 중기, 그리고 후기 처리군에서 각각 45.39%, 38.26%, 43.18%, 그리고 73.33%로 모든 adipogenesis 단계에 따라 유의적인 차이를 나타내었다(Figure 5A). 특히 분화이전(A)과 분화초기(B), 그리고 분화중기(C)에 fisetin을 100 μM 농도로 처리하였을 때 가장 효과적인 지방축적 억제활성을 나타내었다. 위의 Figure 5A의 결과와 유사하게, fisetin을 100 μM의 농도로 처리하였을 때 분화이전(A), 분화초기(B), 분화중기(C), 그리고 분화후기(D)의 모든 처리군에서 대조군과 비교하였을 때 지방축적이 감소한 것을 관찰하였다. 특히 분화초기, 분화전기, 그리고 분화중기에서 지방구의 수와 크기가 크게 감소하는 결과를 나타냈다(Figure 5B). 지방세포는 에너지 항상성 유지 및 지질대사에 중요한 역할을 하며, 3T3-L1 전지방세포는 다양한 호르몬 및 sterol regulatory element-binding protein 1c (SREBP-1c), PPARγ, 그리고 C/EBPα와 같은 지방세포 분화에 중요한 역할을 하는 전사인자들에 의해 지방세포로 분화되는 adipogenesis 과정을 조절하여 세포 내 중성지질을 축적한다(Choi & Kim, 2014). 따라서 adipogenesis 전사인자의 조절은 항비만 활성을 나타내는데 있어 중요하다. 이와 관련해 기 보고된 연구결과로는 감귤류 종인 한라봉(Citrus kiyomi×ponkan) 과피 추출물이 C/EBPα와 PPARγ 등의 전사인자 발현 저해를 통해 항비만 의약품으로 잘 알려진 SinetrolⓇ 양성대조군보다 약 5배 이상의 높은 adipogenesis 억제 활성을 보였으며, 차전초(Plantago asiatica L.) 에탄올 추출물이 3T3-L1세포에서 비만관련 지표인 AMP-activated protein kinase (AMPK)와 지방 생성 및 지방산 산화와 관련된 acetyl-CoA carboxylase (ACC)의 인산화를 유의적으로 증가시킴으로서 지방구의 축적을 억제하고, adipogenesis를 억제한다는 연구가 보고되었다(Jeon et al., 2014; Lim et al., 2014). 또한 연잎-연근 혼합 발효 추출물이 발효하지 않은 추출물에 비해 지방구의 수와 크기를 감소시킴으로서 발효된 연잎-연근 추출물이 adipogenesis를 억제 시킨다는 연구가 보고되었으며(Lee et al., 2013), 플라보노이드, 폴리페놀 등 다양한 항산화 물질이 포함되어있는 소리쟁이(Rumex Crispus L.) 분획물이 adipogenesis를 억제하여 지방구의 수와 크기를 감소시킨다는 결과가 보고되었다(Park et al., 2013). 그러므로 fisetin이 분화이전, 분화초기, 그리고 분화중기에 특이적으로 작용하여 adipogenesis에 있어 중요한 전사인자의 발현조절을 통해 지방구의 축적을 억제하는 것으로 생각된다.
5. RT-PCR를 통한 mRNA 발현수준 평가Fisetin이 3T3-L1 세포에서 adipogenesis를 조절하는 전사인자 및 지방세포 특이적 유전자에는 어떠한 영향을 미치는지 알아보기 위해 세포분화 조건은 Figure 1과 동일하게 실시하였으며 Day 6에 TRIzolⓇ을 사용하여 RNA를 추출하여 RT-PCR을 통해 mRNA의 발현수준을 분석하였다. Fisetin에 의한 C/EBPβ, leptin, 그리고 adiponectin의 mRNA 발현수준은 Figure 6에 나타내었다. 분화되지 않은 전지방세포에 비해 분화된 지방세포에서 각각의 C/EBPβ, leptin, 그리고 adiponectin의 mRNA 발현수준은 크게 증가하였으며, fisetin을 10, 25, 50 그리고 100 μM 농도로 처리하였을 때 대조군에 비해 mRNA 발현수준이 현저히 감소한 것을 확인하였다.
Adipogenesis는 IBMX, dexamethasone, 그리고 insulin를 사용한 호르몬 유도에 의해 C/EBPβ가 발현되고, C/EBPβ의 발현수준의 증가에 뒤이어 C/EBPα와 PPARγ의 발현수준이 증가된다. 많은 유전자들이 C/EBPα와 PPARγ의 발현으로 인해 adipogenesis와 관련된 지방세포 특이적 유전자들이 조절된다고 알려져 있다(Lee et al., 2014; Park et al., 2014). Adipogenesis 과정과 관련된 이전 연구에서는 우엉의 lignan 화합물에서 분리된 arctiin과 함께 고지방식이 섭취된 쥐의 체질량을 감소시키고 PPARγ, C/EBPα SREBP-1c, aP2, 그리고 LPL과 같은 adipogenesis에 관여하는 유전자의 mRNA 발현수준 감소를 통해 adipogenesis를 억제하였다(Min et al., 2014). 또한 녹색입홍합 추출물이 C/EBPα, 그리고 FAS와 같은 전사인자의 mRNA 발현수준을 감소시키고, 분화 후 adipogenesis 과정을 조절함으로서 세포내의 지방축적 억제를 통한 항비만 활성이 보고되었다(Shon et al., 2013). 따라서 fisetin은 3T3-L1 지방세포에서 C/EBP β, leptin 그리고 adiponetin 발현수준을 감소시킴으로서 각각의 adipogenesis 단계에서 지방구 수 및 크기에 억제 효과를 나타내는 것으로 보여진다.
Conclusion비만은 지방세포의 과다한 증식과 에너지 축적의 결과로서 불균형적인 에너지 대사 유발과 심혈관, 뇌혈관 질환, 그리고 암과 같은 다양한 대사성 질병의 원인이 된다. 지방축적은 전지방세포가 성숙한 지방세포로 분화하는 과정인 adipogenesis에 의해 조절되며, 다양한 전사인자에 의해 adipogenesis가 조절된다(Choi et al., 2011). 체내 항산화 시스템은 비만에 의해 산화적 스트레스가 증가되어 각종 질환의 발생위험을 증가시키므로 산화적 스트레스를 억제하고 예방할 수 있는 대책이 필요한 실정이다(Kim et al., 2011). 그러므로 활성산소로 인한 산화적 스트레스를 조절하고 비만 예방에 있어 adipogenesis를 조절하는 것은 건강증진을 위한 중요한 타겟이 되고 있다. Fisetin은 플라보노이드 중 하나로 사과, 양파, 그리고 감 등에 다량으로 함유되어 있다. Fisetin의 항염증, 항종양, 그리고 항암과 같은 다양한 생물학적 활성이 보고되었으나 미용기능식품 소재로서의 사용가능성에 대한 연구는 미비한 실정이다. 그러므로 본 연구에서는 fisetin의 항산화 활성을 평가하고 3T3-L1 세포에서 adipogenesis의 조절을 통해 항비만 활성을 평가하고자 하였다.
본 연구에서는 다음과 같이 요약할 수 있다. 첫째, fisetin의 항산화 활성은 ABTS 라디칼 소거활성 평가를 통해 확인하였으며 L-ascorbic acid와 비교하였을 때 ABTS 라디칼 소거활성이 더 높았다. 둘째, 3T3-L1 전지방세포에 독성이 나타나지 않는 1, 10, 25, 50, 그리고 100 μM fisetin의 농도를 이후 실험에 적용한 결과, 3T3-L1 지방세포내 축적된 triglyceride는 fisetin의 Day -2~6 처리를 통해 농도 의존적으로 억제하였다. 또한 fisetin이 adipogenesis의 분화 전기, 초기, 중기, 그리고 후기 과정 중 분화 전기, 초기 그리고 중기에 효과적으로 지방축적을 억제하였다. 셋째, Day -2~6 fisetin 처리는 adipogenesis의 주요한 전사인자 및 유전자인 C/EBPβ, leptin, 그리고 adiponectin의 mRNA 발현수준을 억제하였다. 이상의 연구결과는 fisetin이 항산화 및 항비만 효과를 지닌 미용기능식품 소재로서 개발될 수 있는 가능성을 보여주는 결과로 생각되며, 추후 fisetin에 대한 세분화 된 adipogenesis 억제활성 평가 및 분자생물학적 신호전달체계를 규명하는 연구가 추가적으로 요구된다.
Figure 1.Scheme of 3T3-L1 differentiation and fisetin treatment.DM: differentiation medium consist of FBS-DMEM, 0.5 mM IBMX, 5.2 μM dexamethasone, and 167 nM insulin.
Post-DM: post-differentiation medium consist of FBS-DMEM and 167 nM insulin.

Figure 2.Scavenging activity of fisetin against ABTS radicals.Scavenging activity of L-ascorbic acid against ABTS radicals (A). Scavenging activity of fisetin against ABTS radicals (B). IC50 of L-ascorbic acid and fisetin against ABTS radicals were 2.91±0.04 μg/mL and 1.35±0.06 μg/mL, respectively.

Figure 3.Effect of fisetin treatment on 3T3-L1 viability.The 3T3-L1 preadipocytes were incubated with 10% BCS-DMEM containing fisetin for 24 h to measure the cell viability. Viability of 3T3-L1 was determined by EZ-cytox assay. 3T3-L1 preadipocytes were quantified using microplate reader at 570 nm. Corresponding letters (asterisks) indicate significant differences by Student’s t-test (*p<.05).
Control: 3T3-L1 preadipocytes; NS: Not significant.
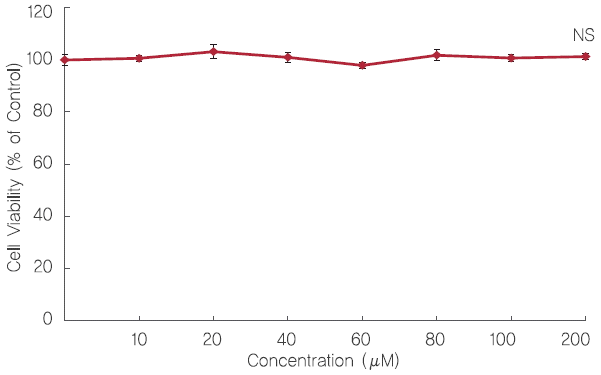
Figure 4.Inhibitory effect of fisetin treatment on the triglyceride content of 3T3-L1 cells.3T3-L1 cells were subjected to adipogenesis in the presence of 1, 10, 25, 50, and 100 μM fisetin during Day -2 to Day 6. Inhibitory effect of fisetin treatment on the triglyceride content in mature 3T3-L1 adipocytes were quantified by EnzyChrom™ triglyceride assay kit. Corresponding letters (asterisks) indicate significant differences by Student’s t-test (*p<.05, and ***p<.001).
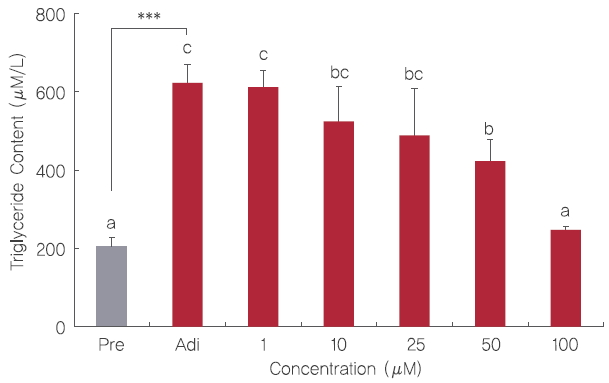
Figure 5.Effect of fisetin treatment on the lipid accumulation of 3T3-L1 adipocytes.Lipid accumulation was evaluated by ORO staining and ORO-stained 3T3-L1 adipocytes were quantified using microplate reader at 510 nm (A). Observation of lipid accumulation in mature 3T3-L1 adipocytes (B). Corresponding letters (asterisks) indicate significant differences by Student’s t-test (**p<.01, and ***p<.001).
Pre: 3T3-L1 preadipocytes; Adi: mature 3T3-L1 adipocytes.
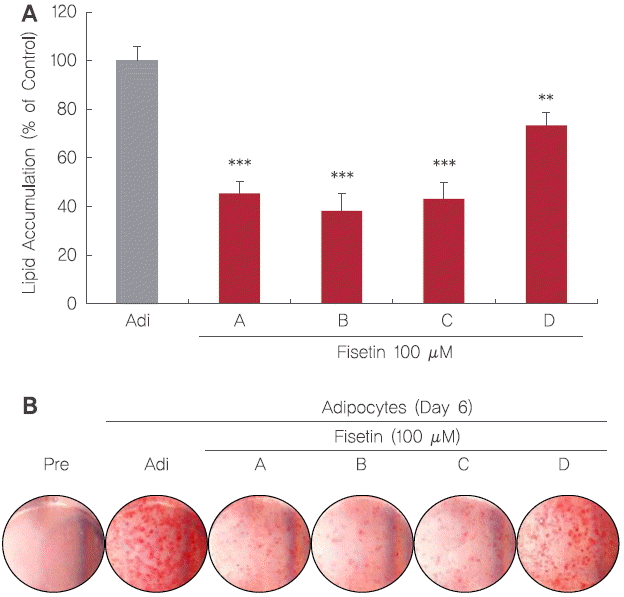
Figure 6.Effect of fisetin treatment on mRNA expression levels of 3T3-L1 adipocytes.3T3-L1 cells were exposed to the 10, 25, 50, and 100 μM fisetin during Day -2 to Day 6. The mRNA expression levels of transcription factors such as C/EBPβ, leptin, and adiponectin was examined by RT-PCR.
Pre: 3T3-L1 preadipocytes; Control: mature 3T3-L1 adipocytes.

References1. Anunciato TP, da Rocha Filho PA. Carotenoids and polyphenols in nutricosmetics, nutraceuticals, and cosmeceuticals. Journal of Cosmetic Dermatology 11: 51-54. 2012.
2. Choi EO, Kim HS, Han MH, Choi YH, Kim BW, Hwang JA, Hwang HJ. Effects of Hizikia fusiforme extracts on adipocyte differentiation and adipogenesis in 3T3-L1 preadipocytes. Journal of Life Science 22: 1399-1406. 2012.
3. Choi HY, Kim GH. Inhibitory effects of Allium senescens L. methanol extracts on reactive oxygen species production and lipid accumulation during differentiation in 3T3-L1 cells. Korean Journal of Food Science and Technology 46: 498-504. 2014.
4. Choi MS, Kim JI, Jeong JB, Lee SB, Jeong JN, Jeong HJ, Seo EW, Kim TY, Kwon OJ, Lim JH. Suppressive effects of by-product extracts from soybean on adipocyte differentiation and expression of obesity-related genes in 3T3-L1 adipocytes. Journal of Life Science 21: 358-367. 2011.
5. Echeverry C, Arredondo F, Martínez M, Abin-Carriquiry JA, Midiwo J, Dajas F. Antioxidant activity, cellular bioavailability, and iron and calcium management of neuroprotective and nonneuroprotective flavones. Neurotoxicity Research 27: 31-42. 2015.
6. Jeon SY, Park JY, Shin IS, Kim SO, An HD, Kim MR. Ethanol extract of Plantago asiatica L. controls intracellular fat accumulation and lipid metabolism in 3T3-L1 adipocytes. The Korea Journal of Herbology 29: 77-82. 2014.
7. Ji HH, Jeong HY, Jin SJ, Kwon HJ, Kim BW. Inhibition of adipocyte differentiation by methanol extracts of Oenanthe javanica seed in 3T3-L1 preadipocytes. Journal of Life Science 22: 1688-1696. 2012.
8. Kim ES, Jang HD, Kim GN. Anti-oxidative function of fisetin and its potential as an anti-oxidant nutri-cosmetics. Korean Journal of Aesthetics and Cosmetology 10: 515-521. 2012.
9. Kim JY, Shin MS, Heo YR. Effects of stabilized rice bran on obesity and antioxidative enzyme activity in high fat diet-induced obese C57BL/6 mice. Journal of the Korean Society of Food Science and Nutrition 43: 1148-1157. 2014.
10. Kim KB, Jang SH. Anti-obesity effect of EGCG and glucosamine-6-phosphate through decreased expression of genes related to adipogenesis and cell cycle arrest in 3T3-L1 adipocytes. Journal of Nutrition and Health 47: 1-11. 2014.
11. Kim MJ, Hong CO, Nam MH, Lee KW. Antioxidant effects and physiological activities of pumpkin (Cucurbita moschata Duch.) extract from different aerial parts. Korean Journal of Food Science and Technology 43: 195-199. 2011.
12. Lee MH, Nam DE, Kim OK, Heo SH, Lee JM. Lipolytic effect of supercritical extraction from pine cone (Pinus koraiensis) in mature 3T3-L1 adipocytes. Journal of the Korean Society of Food Science and Nutrition 43: 1342-1348. 2014.
13. Lee SJ, Bose S, Lee SJ, Jeong JE, Koo BS, Kim DI, Kim HJ. Effects of fermented lotus extracts on the differentiation in 3T3-L1 preadipocytes. Journal of Korean Medicine for Obesity Research 13: 74-83. 2013.
14. Lim HJ, Seo JE, Chang YH, Han BK, Jeong JK, Park SB, Choi HJ, Hwang JA. Anti-obesity effects of Jeju hallabong tangor (Citrus kiyomi×ponkan) peel extracts in 3T3-L1 adipocytes. Journal of the Korean Society of Food Science and Nutrition 43: 1688-1694. 2014.
15. Min BCR, Lee HJ, Song JH, Han MJ, Chung JY. Arctiin inhibits adipogenesis in 3T3-L1 cells and decreases adiposity and body weight in mice fed a high-fat diet. Nutrition Research and Practice 8: 655-661. 2014.
16. Park HJ, Kim AJ, Cheon YP, Lee MS. Anti-obesity effects of water and ethanol extracts of black ginseng. Journal of the Korean Society of Food Science and Nutrition 44: 314-323. 2015.
17. Park JA, Jin KS, Oh YN, Hyun SK, Choi YH, Kown HJ, Kim BW. Antiadipogenic effect of Vitis amurensis root methanol extract and its solvent fractions in 3T3-L1 preadipocytes. Journal of Life Science 23: 69-78. 2013.
18. Park MY, Choi YA, Lee HG, Kim KI, Lim JS, Lee MS, Oh KS, Yang Y. Dephosphorylation of CCAAT/enhancer-binding protein β by protein phosphatase 2A containing B56δ is required at the early time of adipogenesis. BBA Molecular and Cell Biology of Lipids 1841: 1608-1618. 2014.
19. Park SJ, Choi JH, Jung YS, Yu MH. Inhibitory effect of Rumex crispus L. fraction on adipocyte differentiation in 3T3-L1 cells. Korean Journal of Food Science and Technology 45: 90-96. 2013.
20. Park YK, Lee TY, Choi JS, Hong VS, Lee JH, Park JW, Jang BC. Inhibition of adipogenesis and leptin production in 3T3-L1 adipocytes by a derivative of meridianin C. Biochemical and Biophysical Research Communications 452: 1078-1083. 2014.
21. Prasath GS, Subramanian SP. Fisetin, a tetra hydroxy flavone recuperates antioxidant status and protects hepatocellular ultrastructure from hyperglycemia mediated oxidative stress in streptozotocin induced experimental diabetes in rats. Food and Chemical Toxicology 59: 249-255. 2013.
22. Re R, Pellegrini N, Proteggente A, Pannala A, Yang M, Rice-Evans C. Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radical Biology and Medicine 26: 1231-1237. 1999.
23. Seo SH, Jeong GS. Fisetin inhibits TNF-α-induced inflammatory action and hydrogen peroxide-induced oxidative damage in human keratinocyte HaCaT cells through PI3K/AKT/Nrf-2-mediated heme oxygenase-1 expression. International Immunopharmacology 29: 246-253. 2015.
24. Shin OS, Shin YH, Lee KH, Kim GY, Kim KH, Park JK, Ahn JI, Song KY. Inhibition of adipogenesis in 3T3-L1 adipocytes with ethanol extracts of Saururus chinensis. Korean Society for Biotechnology and Bioengineering Journal 27: 381-386. 2012.
25. Shon MS, Kim GN. Anti-oxidant and anti-obese activities of turmeric (Curcuma longa L.) extract in 3T3-L1 cells. Korean Journal of Aesthetics and Cosmetology 12: 169-175. 2014.
26. Shon MS, Kim SK, Lee SC, Kim KN. Anti-obese activity of water extract prepared from green-shelled mussel through regulating adipogenesis. Korean Journal of Aesthetics and Cosmetology 11: 1067-1072. 2013.
27. Subramanian P, Jayakumar M, Singaravel M, Kumar D, Basu P, Jayapalan JJ, Hashim OH. Fisetin, a dietary flavonoid, attenuates hyperammonemia and improves circadian locomotor deficits, redox balance, and astrocytic markers in rats. Journal of Functional Foods 12: 409-419. 2015.
|
|
|||||||||||||||||||||||||||||||||||||