요약목적본 연구에서는 천연소재인 새싹인삼과 차풀의 복합추출물을 이용하여 항산화 및 미백효과를 입증하고, 최적의 원료 표준화 과정을 통해 차별화된 천연 화장품 소재를 개발하고자 하였다.
방법유전분석을 통한 새싹인삼과 차풀 각각의 연구소재를 준비하고, 최적의 항산화 및 미백효과를 갖는 새싹인삼과 차풀 복합추출물의 배합비율, 용매비율, 추출온도 및 추출 시간 등을 결정한 후, 최종 복합추출물로부터 지표성분을 설정하였다.
AbstractPurposeIn this study, we tried to develop differentiated natural cosmetic materials through the standardization of optimal raw materials, and demonstrate complex functionality with anti-oxidative and whitening effects of natural extracts of sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda.
MethodsIn this experiment, the research materials, sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda, were prepared by identification of genetic analysis, complex extracts of sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda were determined to have optimum anti-oxidative and whitening effects by studying the mixture ratio, solvent ratio, extraction temperature, and extraction time. The standard compound was prepared from the final complex extract.
ResultsThe mixture ratio of sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda with optimum anti-oxidative and whitening effects was 1:9, extraction solvent was 30% ethanol, extraction temperature was 80℃ and extraction time was 8 h. The antioxidative activity of the complex extract showed 49.6% 1.1-diphenyl-2-picrylhydrazyl (DPPH) radical scavenging activity at 500 μg/mL. In a tyrosinase inhibitory activity assessment, the complex extract showed 109% tyrosinase inhibitory activity at 2,000 μg/mL. The standard compound was confirmed to be Schaftoside.
ConclusionThis study reveals key conditions for the standardization of manufacturing process to obtain optimal anti-oxidative and whitening effects from complex extracts of sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda. We expect that theuse of industrial cosmetics as raw materials for cosmetics, including Shaftoside, will not be hampered by limitations in industrial use due to international patent disputes and high costs.
Introduction전 세계 천연화장품 시장규모가 꾸준히 성장하고 있는 것과 관련하여 천연화장품 개발이 활발히 이루어지고 있으며 그 중 주름개선, 미백, 항염증 등과 관련된 화장품 생산의 증가율과 점유율이 높게 나타나고 있다(Yoo et al., 2004). 국내에서도 전 세계 동향과 유사하게 미백, 주름개선, 항염증과 관련된 천연화장품 제품이 증가하고 있다(Kim, 2006). 향후 천연화장품은 산업적, 기술적인 성장세가 예상되며 특히 산업현장의 요구와 소비자 선호도가 충분히 확인된 만큼 안전성, 효능 개선 등에 대한 연구결과가 입증된다면 지속적인 발전이 가능할 것으로 예상된다(Choe & Choe, 2014; Han & Yi, 2012).
본 연구 소재인 새싹인삼(sprout Panax ginseng C.A. Meyer)은 천연소재로써 새싹삼 또는 인삼새싹이라고 하며, 2년 미만의 인삼을 2-4개월 수경재배로 키우는 것이 특징이다. 또다른 소재인 차풀은 며느리감나무, 생약명으로는 산편두, 학명으로는 Cassia nomame (Sieb.) Honda로 불리우며, 한국, 중국 등지에 분포하는 콩과의 한해살이 식물로 높이 30-60 cm에 이른다. 잎은 줄모양의 타원형으로 어긋나 자라며, 꽃은 7-8월에 피는 노란색 꽃으로, 열매는 편평한 타원형이다. 종자는 검은색으로 광택이 있고, 냇가 근처의 양지에서 자라며, 결실기는 10월이다. 새싹인삼뿐만 아니라 차풀 역시 식물의 전체부위(일명 전초)가 식용 가능한 원료로써 별도의 화장품 원료 등록 절차 없이 바로 사용이 가능한 천연소재이다(Jo et al., 2011; Lee et al., 2010; Rhim et al., 2009). 따라서 본 연구에서는 천연소재인 새싹인삼과 차풀의 복합추출물을 이용하여 항산화 및 미백효과를 입증하고, 지표물질의 설정을 통해 차별화된 천연화장품 소재를 개발하고자 하였다.
Methods1. 새싹인삼과 차풀 시료준비새싹인삼은 전남 장성군에 위치한 윤희네 농장(Korea)에서 구입하였으며 채취시기 7월-8월에 해당하는 전초를 사용하였다. 차풀은 9월-10월 사이에 채취한 전초를 사용하였으며, 강원도 삼척시 자연약초 농장(Korea)에서 구입하였다. 보통 새싹인삼은 뿌리 부분만을 사용하는 경우가 많았으나 본 연구에서는 뿌리, 줄기 및 잎을 포함하는 새싹인삼의 전 부위를 원료로써 사용하였다(Lee et al., 2010). 차풀 또한 뿌리를 제거하지 않은 전초를 세척한 후 물기를 건조하여 준비하였으며, 건조된 시료는 -20℃ 냉동고에 보관 후 실험에 사용하였다.
2. 새싹인삼과 차풀의 유전분석본 실험에 사용된 새싹인삼과 차풀은 각각 전남 장성 농장과 강원도 삼척에서 구입 후, 세척 및 건조하였으며 DNA 추출 전까지 -80℃에서 보관하여 실험을 진행하였다. Genomic DNA를 분리하기 위해 채취한 시료 0.3 g을 pestle을 사용하여 액체질소 상에서 아주 곱게 간 후 DNeasy Plant mini kit (Qiagen, Germany)를 사용하여 매뉴얼에 따라 DNA를 추출하였다. 추출한 DNA는 NanoDropTM (ThermoFisher Scientific, USA)으로 DNA 정량을 실시하여 50 ng/μL으로 희석하여 polymerase chain reaction (PCR)에 사용하였다. 차풀의 Internal Transcribed Spacer (ITS) 영역을 증폭하기 위해 universal ITS 영역 증폭 primer를 사용하여 PCR을 실시하였다(Chen et al., 2010). PCR 조건은 50 ng/μL genomic DNA, 1U Ex Taq polymerase (TaKaRa), 1×PCR buffer (50 mM KCl, 10 mM Tris-HCl, pH8.3), 200 μM dNTPs, 5 pM forward 및 reverse primer (Table 1)를 넣고 총량을 3차 증류수로 50 μL가 되도록 맞추었다.
반응조건은 먼저 95℃에서 5 min 초기 변성(denaturation)을 한 다음, 95℃에서 30 s 변성(denaturation), 55℃에서 30 s 풀림(annealing), 72℃에서 30 s 확장(extension)하여 40회 반응시킨 후 마지막에 72℃에서 5 min 확장(extension)하였으며, 각 PCR 증폭 산물은 1.5% agarose gel에 전기영동을 하고 UV transilluminator (UVITec Cambridge, UK)를 이용하여 DNA 밴드를 확인하였다.
새싹인삼과 차풀의 18S 유전자의 염기서열을 밝히기 위하여 ITS primer set에 의해 증폭된 PCR 산물(약 700bp)을 QIAquick® Gel extraction kit (Qiagen)를 이용하여 회수하였으며, Enzynomics 사(Korea)의 TOPcloner™ TA kit를 사용하여 매뉴얼에 따라 TA cloning을 진행하였으며 염기서열을 확인하기 위한 sequencing은 Cosmogentech (Korea)에 의뢰하여 진행하였다. 새싹인삼과 차풀의 염기서열은 Mega 7.0 (Edgar, 2004)과 CLC sequence viewer version 6.9 (CLC Bio, Denmark)를 사용하여 NCBI의 GeneBank의 유전자 정보와 multiple alignment를 실시하였고 MEGA 7.0의 최대우도법(maximum likelihood method)으로 계통수를 생성하고 판독하여 계통도를 작성하였다. 계통수에 대한 신뢰도는 부트스트랩(bootstrap) 값을 500회 반복하여 평가하였다(Rhim et al., 2010).
3. 새싹인삼과 차풀 복합추출물의 최적 배합비율새싹인삼과 차풀 복합추출물을 제조하기 위하여 새싹인삼과 차풀의 배합비율(중량 비), 추출 용매, 추출 온도, 추출시간에 따른 항산화 및 미백효과(tyrosinase 저해)를 측정하여 최적의 추출 조건을 확인하였다(Jeon et al., 2015).
항산화와 미백효과가 가장 우수한 새싹인삼과 차풀의 최적 배합비율을 찾기 위하여 새싹인삼과 차풀의 배합비율(중량비)을 3:1, 2:1, 1:1, 1:2, 1:3, 1:4, 1:5, 1:6, 1:7, 1:8 및 1:9로 하여 열수추출을 수행하였다. 열수추출은 80℃에서 8 h 동안 수행하는 조건으로 고정하여 수행하고, 추출된 새싹인삼과 차풀 복합추출물에 대하여 동결건조를 수행한 후 항산화 및 미백효과를 측정하였다.
4. 새싹인삼과 차풀 복합추출물의 최적 추출용매 및 용매비율가장 우수한 항산화 효과를 보이는 배합비율을 선택 후 물, 10% 에탄올(DUKSAN, Korea), 20% 에탄올 및 30% 에탄올을 사용하여 새싹인삼과 차풀 복합추출물을 추출하였다. 추출은 80℃에서 8 h 동안 수행하는 조건으로 고정하여 수행하였으며, 추출된 새싹인삼과 차풀 복합추출물에 대하여 동결건조를 수행한 후 항산화 및 미백효과를 측정하였다.
5. 새싹인삼과 차풀 복합추출물의 최적 추출온도 및 추출시간배합비율과 추출 용매를 결정한 후 온도에 따른 활성을 확인하기 위하여 추출온도를 20℃, 40℃, 60℃, 80℃ 및 100℃로 하고, 8 h 동안 추출하였다. 또한, 최적 추출시간을 확인하기 위하여 2-12 h까지 2 h 간격으로 추출을 수행하였으며, 추출된 새싹인삼과 차풀 복합추출물에 대하여 동결건조를 수행한 후 항산화 및 미백효과를 측정하였다.
6. DPPH 라디칼 소거능 측정새싹인삼과 차풀 복합추출물의 항산화 효능 평가는 Blois 방법을 변형하여 측정하였다(Jeong & Kim, 2016). 각 농도별 희석시료액 20 μL와 0.15 mM DPPH (Sigma-Aldrich, USA) 200 μL를 혼합한 후 30 min 암실 반응하였다. 그 후 microplate reader SpectraMax 190 (Molecular Device, USA)를 이용하여 517 nm에서 흡광도를 측정하는 방법으로 라디칼 소거능을 확인하였다. 소거능은 시료 첨가구와 무첨가구의 흡광도 차이를 백분율(%)로 구하였다.
DPPH 라디칼 소거능(%)=[1-(A/B)]×100
A: 시료 첨가구 흡광도
B: 시료 무첨가구 흡광도
7. Tyrosinase 저해 활성새싹인삼과 차풀 복합추출물의 미백효과는 tyrosinase의 저해 활성을 측정하여 확인하였다. 0.1 M sodium phosphate (pH 6.5) buffer (Junsei, Japan) 220 μL, 시료액 20 μL, 1500 U/mL tyrosinase (Sigma-Aldrich) 20 μL, 1.5 mM tyrosine (Sigma-Aldrich) 40 μL를 순서대로 혼합하고, 혼합액을 37℃에서 10 min 동안 반응시킨 후 490 nm에서 흡광도를 측정하였다(Kwon, 2015).
Tyrosinase 활성 저해율(%)=[100-(B-B'/A-A')]×100
A: 공시료액의 반응 후의 흡광도
B: 시료액의 반응 후의 흡광도
A', B': tyrosinase 대신 0.1 M sodium phosphate (pH 6.5)로 대체하여 측정한 흡광도
8. 지표성분 확인새싹인삼과 차풀 복합추출물에 대하여 high performance liquid chromatography (HPLC) 분석 및 matrix-assisted laser desorption ionization time of flight mass spectrometer (MALDI-TOF/MS) 실험을 수행하여 복합추출물의 지표물질을 설정하였다. 복합추출물은 Triart C18 PLUS column (S-5 μm, 250×4.6 mm l.D.; YMC, Japan)을 이용하여(Hur et al., 2010; Kim et al., 2014), injection volume 10 μL, flow rate 1 μL/min, 온도는 37℃ 조건에서 분석하였다. HPLC system은 pump LC30AD XR, Auto-sampler SIL-20AXR, UV-VIS detector (SPD 20A; Shimadzu, Japan)를 사용하였으며 solvent 조건은 0.01% formic acid (J.T. Baker®, USA)가 포함된 물과 acetonitrile (ACN; J.T. Baker®)로 물과 ACN의 비율을 조절하여 Table 2와 같이 수행하였다. 분획한 후보 지표물질에 대하여 ultra-fast liquid chromatography coupled with ion trap time of flight mass spectrometer (UFLC IT TOF/MS, LCMS-IT-TOF; Shimadzu)를 이용하여 질량분석을 수행하였으며, 이를 데이터베이스에 비교하여 지표물질을 확인하였다.
Results and Discussion1. 새싹인삼과 차풀의 유전분석새싹인삼과 차풀의 유전분석을 위하여 PCR 후 TA cloning 방법(Yang et al., 2012)으로 ITS 염기서열을 확인하였다. 그 결과 새싹인삼은 염기서열의 재배열(multiple alignment)을 통해 고려인삼 품종인 검풍, 고풍과 100%, 춘풍과 99% 이상의 상동성(homology)이 있음을 확인하였다(Rhim et al., 2010). 미국 국립생물정보센터(national center for biotechnology information, NCBI)의 유전자은행(GeneBank)에 등록되어 있는 인삼속(Panax)의 종(species)들과의 계통 분석에서는 새싹인삼이 고려인삼 품종과 같은 분계조를 형성하며 97%의 확률로 유전적 신뢰도를 가지고 있음을 확인하였다. 따라서 새싹인삼은 고려인삼의 품종과 유전적으로 일치함을 확인하였다(Figure 1A).
차풀도 새싹인삼과 동일한 방법으로 염기서열을 재배열하여 Senna nomame HQ833046과 99%의 상동성이 있음을 확인하였다. 또한 미국 국립생물정보센터의 유전자 은행에 등록되어 있는 차풀속(Chamaecrista)의 종(species)들과의 근연 관계를 maximum likelihood method (Tamura & Nei, 1993)로 계통 분석을 실시한 결과, Senna nomame HQ833046와 같은 분계조를 형성하며 100%의 확률로 유전적 신뢰도를 가지고 있음을 확인하였다(Figure 1B). 따라서 실험에 이용한 새싹인삼과 차풀은 기존에 보고되어 있던 고려인삼 및 차풀과 유전적으로 일치함을 확인하였다.
2. 최적 배합비율에 따른 항산화 및 미백효과새싹인삼과 차풀 복합추출물의 최적 배합비율에 따른 항산화 및 미백효능 평가는 DPPH 라디칼 소거능과 tyrosinase 저해활성 평가를 통하여 확인하였다. 최적 배합비율에 따른 항산화 효능 실험 결과, 차풀의 비율이 증가할수록 라디칼 소거능이 증가하였는데 그 중, 새싹인삼과 차풀의 배합비율(중량비)이 1:3, 1:5, 1:9인 복합추출물을 비교하였다. 그 결과 새싹인삼과 차풀의 비율이 1:5보다 1:9에서 라디칼 소거능이 유의적으로 증가하였으며 500 μg/mL의 농도에서 새싹인삼과 차풀의 비율이 1:1, 1:5, 1:9 일 때 라디칼 소거활성이 각각 64.7%, 74.9%, 87.8%의 저해율을 나타내는 것을 확인하였다(Figure 2A; Yoo et al., 2004). 따라서 새싹인삼과 차풀 복합추출물은 차풀의 함량이 증가함에 따라, 복합추출물의 농도가 증가함에 따라 항산화 효과가 함량 및 농도의존적으로 활성이 증가함을 확인하였다.
배합비율에 따른 미백활성 실험결과, 항산화 활성의 측정 결과와 유사하게 새싹인삼과 차풀 비율에 따른 추출물의 미백활성은 배합비율 1:1보다 1:5에서 유의적으로 효능이 향상되는 것을 확인하였으며, 500 μg/mL의 농도에서 비교한 결과, 새싹인삼과 차풀의 비율이 1:1, 1:5, 1:9 일 때 미백활성은 6%, 13%, 22%의 활성을 나타내었다(Figure 2B; Han & Jung, 2003). 차풀 함량이 증가할수록, 복합추출물의 항산화 및 미백효능이 농도 의존적으로 향상됨을 확인하였다.
3. 최적 용매비율에 따른 항산화 및 미백효과추출 용매 및 비율에 따른 항산화, 미백효과는 0%, 10%, 20% 및 30% 에탄올로 추출 후 라디칼 소거능을 확인하였다. 항산화 효능 시험 결과, 10% 에탄올 추출물과 30% 에탄올 추출물의 항산화 효능을 비교하였을 때 복합추출물의 항산화 효과가 유의적으로 증가함을 확인하였다(Figure 3A). 100-1,000 μg/mL 농도에서는 0% 에탄올에 비해 10% 에탄올 추출 시 항산화 효능이 증가하였고, 그 중 100 μg/mL에서는 에탄올의 함량이 증가할수록(10-30%) 항산화 효능이 증가함을 확인하였다. 하지만 500-1,000 μg/mL에서는 10-30% 에탄올 추출 시 활성의 차이를 크게 나타내지 않았다. 실험 결과 저농도(100 μg/mL)에서 복합추출물 추출 시 에탄올의 함량이 증가할수록 항산화 활성이 증가함을 확인하였다.
추출용매 및 비율에 따른 미백효과는 100-500 μg/mL 농도에서 20% 에탄올보다 30% 에탄올 추출 시 복합추출물의 미백효과가 유의적으로 증가함을 확인하였다(Figure 3B). 따라서 새싹인삼과 차풀의 배합비율이 1:9인 경우, 최적의 항산화 및 미백효과를 가지는 추출용매는 30% 에탄올인 것으로 확인하였다.
4. 최적 추출온도에 따른 항산화 및 미백효과새싹인삼과 차풀 추출 시 추출온도에 따른 효능을 확인하기 위하여 20℃, 40℃, 60℃, 80℃, 100℃ 추출 후 항산화와 미백 효과를 측정하였다. 항산화 효능 평가 결과, 500-1,000 μg/mL에서 60℃와 비교하였을 때 80℃로 추출 시 복합추출물의 라디칼 소거능이 유의적으로 증가하였으며 항산화 활성이 매우 좋음을 확인하였다. 그러나 추출온도가 80℃에서 100℃로 증가 시 모든 농도에서 라디칼 소거능이 오히려 감소함을 확인하였다(Figure 4A).
추출 온도에 따른 미백효능은 1,000-2,000 μg/mL에서 40℃와 80℃ 추출물의 효능을 비교하였을 때 80℃로 추출 시 유의적으로 활성이 증가함을 확인하였다. 500 μg/mL에서는 60℃, 1,000-2,000 μg/mL에서는 80℃에서 추출 시 높은 미백 효능을 나타내었지만, 추출온도가 80-100℃로 높아지면 복합추출물의 미백효과는 항산화 효능과 동일하게 오히려 감소하는 것을 확인하였다(Figure 4B; Han & Jung, 2003).
항산화 효능 및 미백활성 효능 실험 결과, 미백 효능은 500 μg/mL에서 60℃ 추출 시 가장 높았으나 고농도(1,000-2,000 μg/mL)에서는 80℃에서 좋은 활성을 나타내었으며, 항산화 효능 또한 500-1,000 μg/mL에서 80℃ 추출 시 높은 활성을 나타내었다. 따라서, 새싹인삼과 차풀의 배합비율 1:9, 추출용매 30% 에탄올인 경우, 최적의 항산화 및 미백효과를 가지는 추출 온도는 80℃로 결정하였다.
5. 최적 추출시간에 따른 항산화 및 미백효과복합추출물의 최적 추출 시간을 확인하기 위하여 2-12 h 동안 2 h 간격으로 추출물을 회수하여 항산화 및 미백 효능을 평가한 결과, Figure 5A에서 보는 바와 같이 복합추출물의 라디칼 소거능은 100-1,000 μg/mL 농도에서 6 h 추출 시 높은 소거능을 나타내었으며, 500-1,000 μg/mL에서 4 h-6 h을 비교한 결과 농도의존적으로 항산화 효능이 증가함을 확인하였다. 하지만 2,000 μg/mL에서는 추출시간에 상관없이 효능의 차이를 보이지 않았다.
미백효과의 경우 100-500 μg/mL에서는 추출 시간에 따른 활성이 큰 차이를 나타내지 않았으나 1,000 μg/mL 농도에서는 6 h, 2,000 μg/mL 농도에서는 8 h 추출한 복합추출물이 가장 우수한 미백효과를 나타냈다(Figure 5B). 그러나 복합추출물 2,000 μg/mL 농도에서 6 h 추출물과 8 h 추출한 복합추출물의 미백효과를 비교하였을 때 유의적으로 미백활성이 증가하였으며 2,000 μg/mL 농도에서 각각 77.9%, 109%의 효능을 나타내었고, 8 h 추출 시 더 향상된 미백효과를 보이는 것으로 판단된다. 따라서 새싹인삼과 차풀의 배합비율 1:9, 30% 에탄올, 80℃로 추출 할 경우 최적의 항산화 및 미백효과를 가지는 추출시간은 8 h으로 확인하였다.
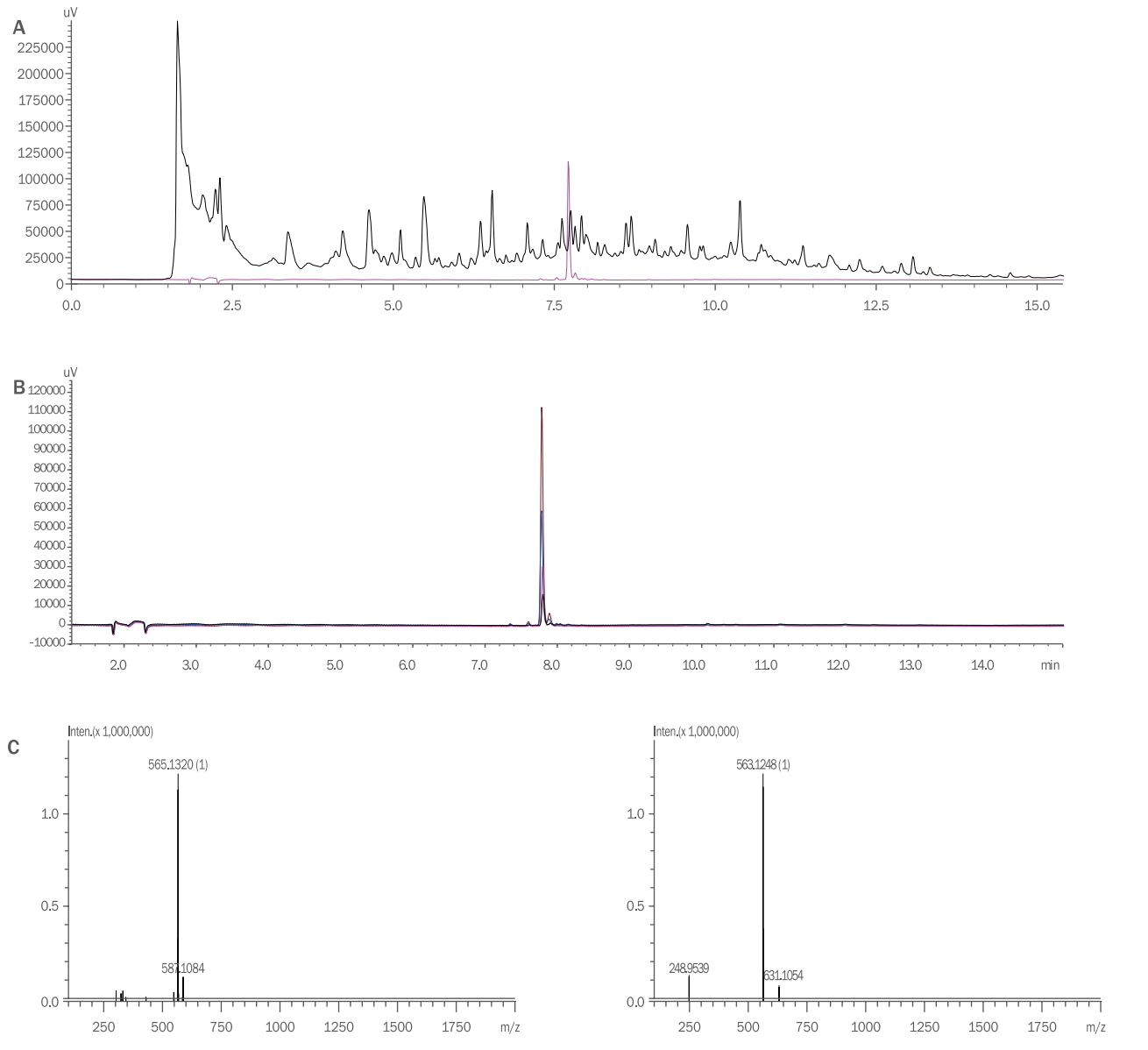
6. 지표성분 확인새싹인삼과 차풀 복합추출물에서 지표성분을 설정하기 위하여 HPLC를 이용하여 복합추출물과 Chemface (China)에서 구입한 샤프토사이드의 피크를 비교 분석하였다. 그 결과, 추출물에서 샤프토사이드와 동일한 시간대에 피크를 확인하였으며(Figure 6A), 복합추출물에서 분리한 물질이 샤프토사이드와 동일 물질임을 확인하기 위하여 injection volume 10 μL, flow rate 1 μL/min, 37℃ 조건에서 Triart C18 PLUS column을 이용하여 분석하였을 때 추출물에서 설정한 물질이 샤프토사이드와 일치함을 확인하였다(Figure 6B). 추출물에서 단일 피크의 분자량 분석 결과, 샤프토사이드와 동일한 563 g/mol 임을 확인하였고(Figure 6C), 기존 라이브러리와 비교하였을 때 샤프토사이드(Schaftoside)와 동일한 물질임을 확인하였다. 샤프토사이드는 최근 천연화장품 조성물의 유효성분으로서 주목 받고 있으며 저농도에서 월등히 우수한 콜라겐 합성 촉진 효과, 항산화 효과, 항염증 효과 및 미백 효과를 나타내므로 피부 재생, 주름 개선, 항산화, 항염증 및 피부 미백을 위한 의약품, 화장료, 건강식품 등의 유효성분으로 사용 가능한 성분으로 알려져 있다(Woo & Woo, 1989). 따라서 샤프토사이드가 포함된 새싹인삼 차풀 복합추출물은 항산화 및 미백에 중요한 역할을 하는 것으로 판단된다.
Conclusion샤프토사이드 또는 이소샤프토사이드는 시계초(passionflower) 또는 석송강(Lycopodiella cernua)에서 추출된 물질에서 확인되는 유효성분이며, 미국 동부가 원산지로 미국 최 남부 및 하와이 등 열대지방에서 자생한다. 석송강은 한국의 전라남도 완도에서도 자생하는 것이 확인되었으나 수십 년 만에 발견될 만큼 귀한 식물이다. 기존에는 샤프토사이드를 추출하여 사용하기 위해서는 석송강만을 사용하여야 했기 때문에 나고야의정서에 따라 국제적인 분쟁이 발생할 우려가 있거나 식물을 구하기가 어려워 생산비용이 상승하는 문제점이 있었다.
본 연구에서는 이러한 문제점을 보완하기 위하여 국내 자생 새싹인삼과 차풀 복합추출물을 이용하여 실험을 진행하였다. 새싹인삼과 차풀의 혼합물에 대하여 열수추출 시 샤프토사이드를 지표물질로 하는 복합물질을 추출 할 수 있으며, 복합추출물이 뛰어난 항산화 및 미백효과가 있다는 것을 실험결과를 통해 확인하였다. 또한 배합 비율, 추출용매, 온도, 시간에 따른 추출법을 확립하였다. 새싹인삼과 차풀 배합비율은 1:9, 30% 에탄올, 80℃, 8 h 추출 하였을 때 뛰어난 항산화 및 미백효능을 검증하였지만, 지표물질로 설정한 샤프토사이드가 새싹인삼 혹은 차풀 중 어디에서 유래한 것인지에 대하여는 추가적인 실험이 필요할 것으로 사료된다. 특히 유용한 천연화장품 원료로 주목 받고 있는 샤프토사이드를 포함하는 복합추출물을 새싹인삼 및 차풀로부터 추출하고 이를 산업적으로 이용한다면 국제적인 분쟁이나 고비용으로 인한 산업적 이용의 제한으로부터 자유로울 수 있을 것으로 기대된다.
Figure 1.Molecular phylogenetic analysis of sprout Panax ginseng and Cassia nomame using a maximum likelihood method.(A) NCBI BLAST search of sprout Panax ginseng C.A. Meyer (JINR 1), (B) NCBI BLAST search of Cassia nomame (Sieb.) Honda (JINR 2).
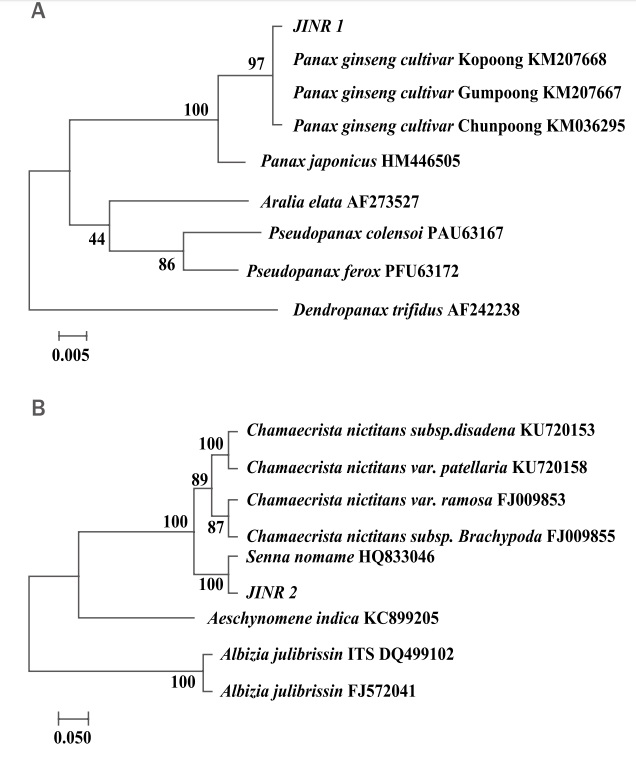
Figure 2.DPPH radical scavenging activity (A) and tyrosinase inhibitory activity (B) by combination ratio of complex extracts using sprout Panax ginsen g C.A. Meyer: Cassia nomame (Sieb.) Honda.Extracts were freeze-dried, and dissolved in 50% DMSO. Diluted extracts were mixed with 0.15 mM DPPH in methanol. After 30 min incubation at room temperature, read the absorbance at 517 nm. Mush room tyrosinase was mixed with 220 μL of phosphate buffer (0.1 M, pH 6.5) and 40 μL of 1.5 mM tyrosine and 20 μL of different concentrated extracts. The mixture was then incubated for 15 min at 37°C. Following incubation, absorbance of the mixture was determined at 490 nm. DPPH radical scavenging activity and tyrosinase inhibitory activity by combination ratio of complex extracts showed relatively high DPPH and tyrosinase inhibitory activity. Each bar indicates the mean±standard deviation (SD) of determinations (n=3). Statistical analysis was performed with a one-way ANOVA (*p<0.05). DPPH, 1.1-diphenyl-2-picrylhydrazyl; DMSO, dimethyl sulfoxide.
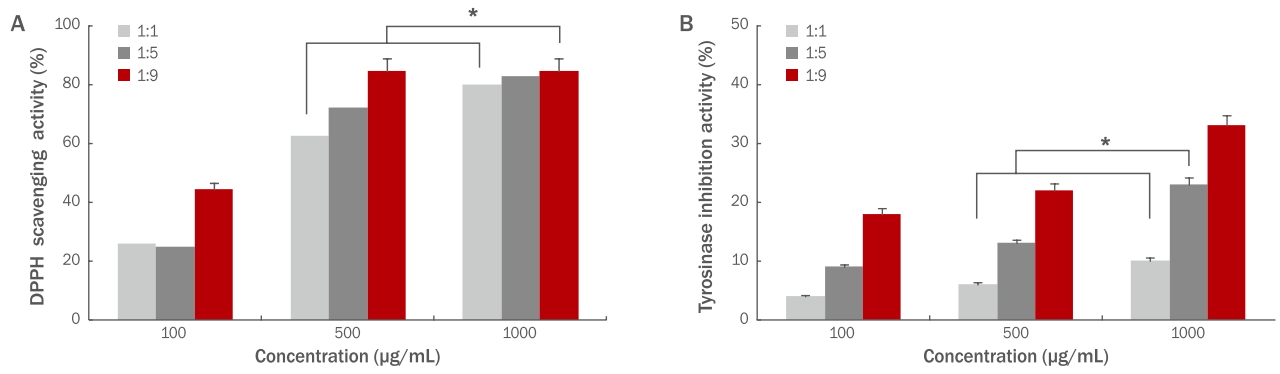
Figure 3.DPPH radical scavenging (A) and tyrosinase inhibitory activity (B) by solvent ratio of complex extracts using sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda.Extracts were freeze-dried and dissolved in 50% DMSO. Each solvent ratio of complex extracts at various concentrations (100, 500, 1,000 μg/mL) was interacted with DPPH and tyrosinase inhibitory activity. DPPH radical scavenging activity and tyrosinase inhibitory activity by solvent ratio of complex extracts showed relatively high DPPH and tyrosinase inhibitory activity. Each bar indicates the mean±standard deviation of determinations (n=3). Statistical analysis was performed with a one-way ANOVA (*p<0.05). DPPH, 1.1-diphenyl-2-picrylhydrazyl; DMSO, dimethyl sulfoxide.
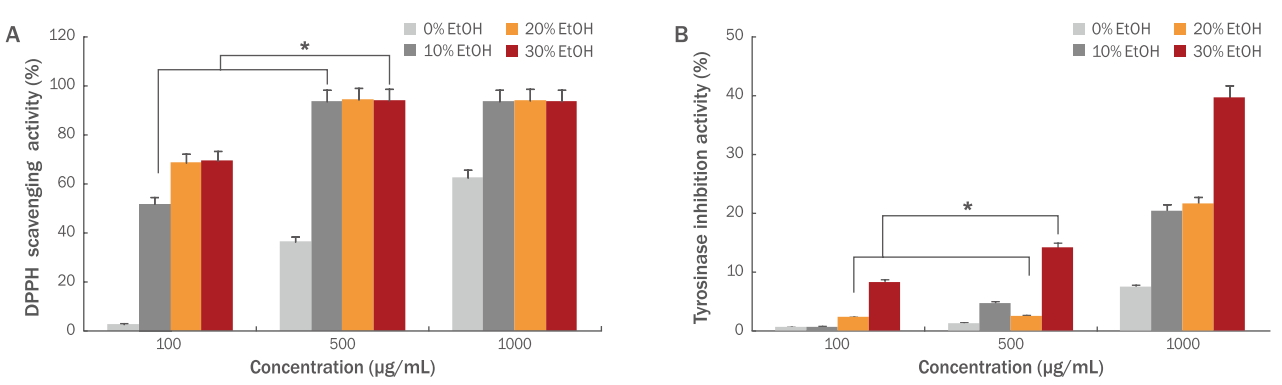
Figure 4.DPPH radical scavenging (A) and tyrosinase inhibitory activity (B) by temperature of complex extracts using sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda.Extracts were freeze-dried and dissolved in 50% DMSO. Each extraction temperature at various concentrations (500, 1,000, 2,000 μg/mL) was interacted with DPPH and tyrosinase inhibitory activity. DPPH radical scavenging activity and tyrosinase inhibitory activity by temperature were displayed in a dose-dependent manner. Each bar indicates the mean±standard deviation of determinations (n=3). Statistical analysis was performed with a one-way ANOVA (*p<0.05). DPPH, 1.1-diphenyl-2-picrylhydrazyl; DMSO, dimethyl sulfoxide.
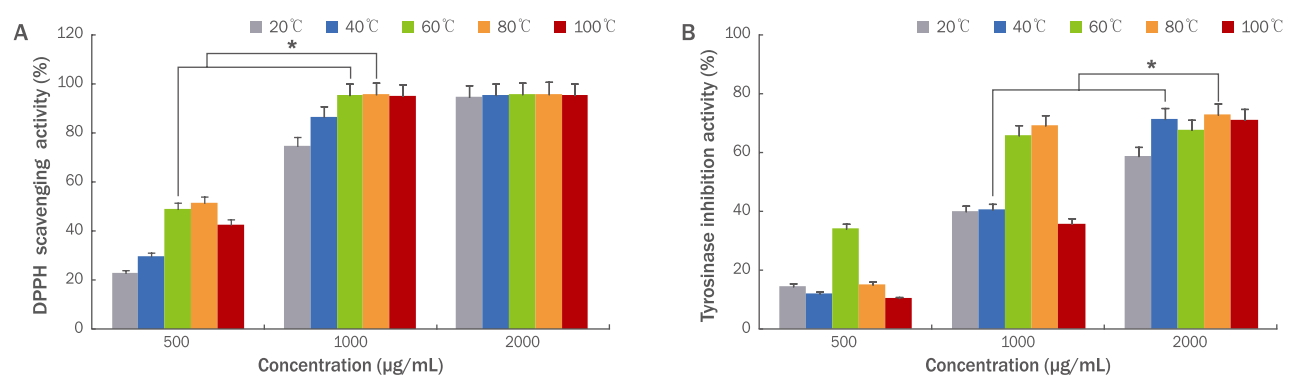
Figure 5.DPPH radical scavenging (A) and tyrosinase inhibitory activity (B) of complex extracts using sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda as a function of time.Extracts were freeze-dried and dissolved in 50% DMSO. Each extraction time at various concentrations (100, 500, 1,000, 2,000 μg/mL) was interacted with DPPH and tyrosinase inhibitory activity. DPPH radical scavenging activity and tyrosinase inhibitory activity by extraction time was displayed in a dose-dependent manner. Each bar indicates the mean±standard deviation of determinations (n=3). Statistical analysis was performed with a one-way ANOVA (*p<0.05). DPPH, 1.1-diphenyl-2-picrylhydrazyl; DMSO, dimethyl sulfoxide.

Figure 6.Screening of standard compound (A) HPLC analysis for Schaftoside (B) and molecular weight analysis using MALDI-TOF/MS of Schaftoside (C) of final complex extract using sprout Panax ginseng C.A. Meyer and Cassia nomame (Sieb.) Honda.Acetonitrile and water were used as mobile phases. A Triart C18 PLUS column (5 μm, 250×4.6 mm) was used to separate the molecules. HPLC-separated fractions were analyzed by mass spectrometry to determine molecular weights. HPLC, high performance liquid chromatography; MALDI-TOF/MS, matrix-assisted laser desorption ionization time of flight mass spectrometer.
ReferencesChen S, Yao H, Han J, Liu C, Song J, Shi L, Zhu Y, Ma X, Gao T, Pang X, et al. Validation of the ITS2 region as a novel DNA barcode for identifying medicinal plant species. PLOS ONE 5: e8613. 2010.
Choe Y, Choe TB. Melanogenesis inhibitory effects of Allium hookeri extract in B16F10 mouse melanoma cell. Asian Journal of Beauty and Cosmetology 12: 163-168. 2014.
Edgar RC. MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Research 32: 1792-1797. 2004.
Han JS, Yi DH. Effects of pine needles fermentation extracts on antioxidant activity and inhibition of melanin synthesis. Asian Journal of Beauty and Cosmetology 10: 619-624. 2012.
Han YS, Jung ES. A study of correlation between antioxidant activity and whitening effect of plant extracts. Asian Journal of Beauty and Cosmetology 1: 11-22. 2003.
Hur SJ, Park EY, Ann MJ, Jang AR, Yang KS, Whang WK. A study on the whitening effects and HPLC pattern analysis of Cirsium setidens Nakai. Asian Journal of Beauty and Cosmetology 8: 1-9. 2010.
Jo JE, Kim KH, Kim MS, Choi JE, Byun MW, Yook HS. Antioxidant activity from different root parts of 6-year-old Panax gingeng C.A. Meyer (Yun-poong). Journal of the Korean Society of Food Science and Nutrition 40: 493-499. 2011.
Jeon KM, Park KH, Pyo AJ. A research on cell proliferation effect and antioxidant activity of extracts based on different extraction methods of Salvia miltiorrhiza Bunge and Scutellaria baicalensis. Asian Journal of Beauty and Cosmetology 13: 495-502. 2015.
Jeong GH, Kim TH. Free radical scavenging and α-glucosidase inhibitory effects of a roots extract of Aruncus dioicus var. kamtschaticus. Korean Journal of Food Preservation 23: 989-994. 2016.
Kwon HJ. Anti-melanogenesis activity of Pleurotus eringii extracts. Asian Journal of Beauty and Cosmetology 13: 695-700. 2015.
Kim EH. A study of whitening cosmetics from natural products. Asian Journal of Beauty and Cosmetology 4: 195-203. 2006.
Kim JW, Moon JS, Choe TB. Comparison of antioxidant activity of Kenaf extract and its flavonoids. Asian Journal of Beauty and Cosmetology 12: 203-210. 2014.
Kumar S, Stecher G, Tamura K. MEGA7: molecular evolutionary genetics analysis version 70 for bigger datasets. Molecular Biology and Evolution 33: 1870-1874. 2016.
Lee HJ, Suh HJ, Lee HS. A study on the utilization of enzyme treated ginseng leaf for cosmeceutical ingredient. Asian Journal of Beauty and Cosmetology 8: 59-69. 2010.
Rhim SY, Choi HJ, Ryu TS, Kwon TR, Choi JK, Sohn JK. Analysis of major traits for native ginseng (Panax ginseng C.A. Meyer) collected from Poonggi area in Korea using DNA marker. Korean Journal of Crop Science 55: 253-258. 2010.
Rhim TJ, Jeong H, Kim YJ, Kim DY, Han YJ, Kwon H, Kwon KR. A study on the comparison of antioxidant effects among cultivated ginseng, and cultivated wild ginseng extracts. Journal of Pharmacopuncture 12: 7-12. 2009.
Tamura K, Nei M. Estimation of the number of nucleotide substitutions in the control region of mitochondrial DNA in humans and chimpanzees. Molecular Biology and Evolution 10: 512-526. 1993.
Woo EH, Woo WS. Flavonoid glycosides from Melandrium firmum. Archives of Pharmacal Research 12: 223-225. 1989.
Yang DH, Maeng S, Strain AK, Floyd A, Nielsen K, Heitman J, Bahn YS. Pleiotropic roles of the Msi1-like protein Msl1 in Cryptococcus neoformans. Eukaryotic Cell 11: 1482-1495. 2012.
Yoo YG, Joung MS, Lee YH, Choi JW, Kim JH, Paek KY. A study on the effect of mountain ginseng adventitious roots extract. Journal of the Society of Cosmetic Scientists of Korea 30: 377-383. 2004.
|
|
|||||||||||||||||||||||||||||||||||||