요약목적최근 화장품 산업의 핵심 원료에 대한 천연 추출물 및 천연 유래 성분에 대한 수요가 증가하고 있으나 그 제조 및 품질 관리 기준이 충분히 확립되어 있지 않다. 본 연구에서는 Chrysanthemum indicum (CI) 및 Cymbopogon cirtratus (CC)의 에탄올 추출물을 사용하여 천연 화장품 조성물의 지표 성분을 표준화하고 분석방법을 확립하고자 하였다.
방법LC/MS 분석을 통해 정량 분석을 위한 지표 성분으로 astragalin과 p-coumaric acid를 선정하였다. HPLC-DAD를 사용하여 두 추출물의 혼합조성물에서 지표 성분을 동시에 분석했다. HPLC-DAD를 사용하여 직선성, 정확성 및 정밀성 분석을 수행했다.
AbstractPurposeRecently, the demand for natural extracts and naturally derived ingredients from core raw materials has increased in the cosmetic industry, but their manufacturing and quality control standards are not sufficiently established. This study aims to standardize the compositions of marker compounds from natural cosmetics using ethanol extracts of Chrysanthemum indicum (CI) and Cymbopogon cirtratus (CC). The method is then validated.
MethodsIn liquid chromatography (LC)/mass spectrometry, astragalin and p-coumaric acid were determined as the marker compounds for quantitative analysis. The performances (linearity, accuracy, and precision) of these two marker components were simultaneously analyzed in a mixture of both natural products using high-performance liquid chromatography with a diode array detector (HPLC-DAD).
ResultsThe marker compounds of CI and CC in the extracts were determined as astragalin and p-coumaric acid, respectively. The detected marker compounds from the CI and CC showed significant linearity (R2≥0.9999). The astragalin and p-coumaric acid markers achieved limits of detection of 1.20 and 0.07 ng/mL, respectively, and limits of quantification of 3.59 and 0.22 ng/mL, respectively. The marker concentrations were 0.24 μg/mL in CI and 1.55 μg/mL in CC.
中文摘要目的 近年来,化妆品行业对核心原料中天然提取物和天然衍生成分的需求有所增加,但其制造和质量控制标准尚未得到充分确立。这项研究旨在使用菊花(Chrysanthemum indicum, CI)以及柠檬草(Cymbopogon cirtratus, CC)的乙醇提取物标准化天然化妆品中标志物的组成。 然后验证该方法。
方法 在LC/MS中,黄芪素和对香豆酸被确定为定量分析的标志物。使用带有二极管阵列检测器的高效液相色谱法(HPLC-DAD),同时在两种天然产物的混合物中分析了这两种标记物组分的性能(线性,准确度和精密度)。
Introduction화장품 구매에 있어 성분이 주요 결정 요인으로 부상하는 가운데, 소비자들의 화학물질 공포증(chemical phobia)이 심해지며 천연 원료에 대한 수요가 증가하고 있다. 또한, 소비자들은 천연제품을 선호하면서도 여러 가지 효능을 갖춘 기능성을 원하기 때문에, 이를 뒷받침할 기능성 화장품 소재 개발이 요구된다. 최근, 국내에서도 지역 특화 기능성 소재 개발이 시도되고 있다. 그 중 한 예로, 말 사업 특구로 지정된 제주의 말 부산물을 활용하여 피부 건강 증진 효과가 있는 펩타이드를 분리하는 원천 기술을 개발하여, 화장품 업체에 기술을 이전한 사례가 있다. 이러한 기능성 천연 추출물 또는 천연 유래 화합물로 환경/인간 친화적인 화장품 천연 소재를 개발해 적용하는 기술이 필요하다.
천연 화장품은 천연물을 사용하여 부작용이 적고, 작용이 일반적으로 온화, 지속적이며 생분해성이 높아 환경친화적인 장점이 있으나, 유효성분 또는 약리작용이 밝혀지지 않거나 유효성분의 함량이 일정하지 않아 원료물질의 유효성분의 함량을 정확하게 특정할 수 없으면 제품의 기능성에 대한 신뢰도를 얻기가 어려우며, 이를 위한 소재에 관한 개선 연구가 필요한 실정이다(Bae, 2017; Ahn, 2017).
감국(甘菊)은 국화과의 여러해살이풀로 황국(黃菊)이라고도 하며 생약명으로는 야국화(野菊花), 의화(義花), 야황국(野黃菊)이라 한다(Kim, 1998). 동의보감에서 감국은 풍으로 어지럽고 머리가 아픈 것을 치료하며, 예막을 없애고 눈을 밝게 하며 눈의 피를 길러주고 내장을 치료하며 바람이 불면 눈물이 나는 것을 멎게 한다고 기록되어 있다(Heo, 2008). 한방에서 열감기, 폐렴, 기관지염, 두통, 위염, 장기, 종기 등의 치료에 처방한다. 보고된 활성으로는 노화와 주름 생성 경감(Kim, 2016) 항암 활성, 산화스트레스 저해, 항산화 활성, 결핵균 및 바이러스 등에 대한 항박테리아 효과 등이 보고되어 있다(Kim et al., 2005; Park et al., 2011; Woo et al., 2010). 감국의 성분으로는 eugenol, isoeugenol, cynaroside, apigetrin 등이 보고되어 있다(Hyun et al., 2019).
레몬그라스(Cymbopogon cirtratus)는 향아(香芽)라는 이름이 있지만, 통상적으로는 레몬그라스로 불린다. 향료를 채취하기 위하여 열대지방에서 재배하며 레몬 향이 나는 허브의 일종으로 외떡잎식물 벼목 화본과의 여러해살이풀이다. 레몬그라스는 잎과 뿌리를 증류하여 얻은 향유(香油)에는 시트랄(citral)이 들어있어 비누와 약품 등의 향료로 사용한다. 수프, 소스 등과 같은 요리에도 사용되며, 살균작용이 있어 복통, 설사, 두통, 발열의 치료에 사용된다. 보고 된 활성으로는 피부보습 및 피부장벽개선(So et al., 2019), 항산화, 지방세포 분화 억제효과, 항암, 항염증 활성 등이 보고 되어있으며(Bhattacharya, 1998; Francisco, 2014), 성분으로는 α-pinene, camphene, limonene, myrcene, citral 등이 보고 되어있다(Jo et al., 2019).
본 연구 그룹은 기존 선행연구에서 기능성 천연 화장품 소재의 개발 및 원료 표준화를 위해 남원에서 자생하는 허브 및 외래종으로 재배하고 있는 천연물 원료의 10종에 대한 항산화 활성 평가 및 그 중 산구절초, 자소엽, 찔레의 동시 분석을 통한 유효성분을 정량 평가하였다(Ham et al., 2018). 본 연구에서는 총 플라보노이드와 폴리페놀함량이 높은 소재인 감국 (Chrysanthemum indicum, CI)과 레몬그라스(Cymbopogon cirtratus, CC)를 선정하여 DPPH 라디칼소거능 평가 및 HPLC-DAD를 이용한 지표 성분의 동시 분석법을 개발하였다. 또한, 이의 타당성을 검증하기 위해 직선성, 범위, 특이성, 정확성, 정밀성, 검출한계 등의 분석법 밸리데이션을 수행하였다.
본 연구에서 수립한 분석법 밸리데이션을 활용하여 감국, 레몬그라스를 함유하는 천연화장품의 개발단계부터 제품생산 단계에 이르기까지 원료소재의 품질관리와 제조관리에 응용할 수 있을 것으로 사료된다.
Methods1. 실험 재료감국(CI)과 레몬그라스(CC)의 지상부를 전라북도 남원시에서 5월에 수확한 생물로 구입하였다. 40℃에서 72 h 건조(LD9013; L'EQUIP Co., Korea)한 후, 분쇄기(HMF-3600TG; Hanil Electric, Korea)를 이용하여 분쇄하여 100 g에 50% 에탄올 2 L를 넣어 80℃에서 4 h 동안 추출하였다. 그 후, 추출물은 2회 여과하여 감압농축기(R100; BUCHI, Switzerland)를 이용하여 50℃에서 농축하고 동결건조(MCFD8508; IlshinBiobase Co., Korea)하여 시료로 사용하였다. 추출 수율은 약 17% 이었다.
2. 시약표준품 astragaline, p-coumaric acid는 HPLC grade (순도 98% 이상)로 Chengdu Biopurify Phytochemicals (Chengdu, China)에서 구입하여 사용하였다. Acetonitrile, methanol, water는 J.T Banker (Phillipburh, USA)에서, formic acid는 Fluka (Wunstorfer strasse, Germany)에서 구입하였으며, 분석에 사용한 모든 시약은 HPLC grade를 사용하였다.
3. DPPH 라디칼 소거 활성2,2-diphenyl-1-picryldrazyl (DPPH) 라디칼 소거 활성은 Blois법(Blois, 1958)을 변형하여 측정하였다. 일정 농도로 희석한 시료 2.5 µL에 10 µM DPPH (Sigma Aldrich, USA) 용액 247.5 µL를 더한 뒤, 차광하여 실온에서 20 min 반응시킨 후 ELISA Reader (Bio-Rad Heciles, USA)를 사용하여 517 nm에서 흡광도를 측정하였다. 각 시료는 3회 반복 실험을 실시한 뒤, 각 시료의 활성이 50% 감소할 때 나타나는 시료의 농도(RC50)를 구하였다. 양성대조군은 L-ascorbic acid (Amresco, USA)를 사용하였다.
4. 분석 시료의 전처리HPLC 분석을 위한 시료는 100 mg을 취해 10 min, 50% 에탄올 1 mL로 초음파 추출한 뒤, 0.2 µm membrane filter (PALL Co., USA)로 여과하여 사용하였다. 지표 성분의 표준품은 각각의 표준품을 10 mg을 100 µL의 50% 에탄올에 녹인 뒤, 0.2 µm membrane filter (PALL Co.)로 여과하여 사용하였다. 시료의 희석은 10% 에탄올로 희석한 뒤 분석하였다.
5. HPLC 분석 조건지표 성분의 함량을 분석하기 위하여 Hitachi Chromaster HPLC CM5000 system (Hithachi, Japan)을 사용하였으며, 검출기는 Diode assay detector (DAD)를 사용하였다. 칼럼은 YMC-Pack ODS-AM, C18 250×4.6 mm I.D. (YMC, Japan)를 사용하였다. 칼럼 온도는 40℃로 유지하였고, 유속은 1.0 mL/min 조건으로 분석했다. 이동상은 0.1% formic acid가 함유된 DW (A)와 0.1% formic acid가 함유된 acetonitrile (B)을 사용하였으며 이동상의 기울기는 0-2 min, (A): 100% 2-50 min (A): 60%, 50-55 min, (A): 0%, 55-60 min, (A): 0%, 60-65 min, (A): 100%, 65-70 min, (A): 100%로 분석했다. 검출 파장은 237 nm와 248 nm에서 검출하였다. HPLC 데이터 분석은 Agilent Open Lab software를 사용하였다(Lee, 2018).
6. 분석법 밸리데이션확립된 동시 분석법에 대하여 식약처에서 고시한 의약품 밸리데이션 가이드라인에 따라 직선성(linearity), 범위(range), 검출한계(LOD), 정량한계(LOQ), 정확성(accuracy), 정밀성(precision)등을 판단하여 분석방법을 검증하였다(NIFDS, 2015; KFDA, 2008; Yong, 2019).
7. 직선성 및 범위지표 성분들을 네 가지 농도(0.1, 1, 10, 50 µg/mL)로 희석하여 3회 분석 후 얻은 결과를 가지고 표준 검량선(calibration curve) 및 회기방정식(regression equation)을 작성하여 직선성을 평가했다.
8. 특이성감국, 레몬그라스 50% 에탄올추출물의 혼합물과 각각의 지표 성분들을 혼합한 표준품 혼합액을 제조한 뒤, 분석하여 얻은 크로마토그램을 시각적으로 평가하고, 해당 지표 성분의 UV 스펙트럼을 시료와 표준품의 혼합액의 크로마토그램에서 추출하여 비교하는 것으로 평가하였다.
9. 정확성 및 정밀성정확성과 정밀성 모두 지표 성분의 피크의 적분 값을 비교하는 방법으로 측정하였다. 정확성은 세 가지 농도의 표준품을 시료에 첨가하여 분석한 후 회수율을 측정하는 방법으로 평가하였고, 정밀성은 균일한 검체로부터 여러 번 채취하여 얻은 시료를 정해진 조건에 따라 측정하였을 때 각각의 측정값들 사이의 근접성으로 상대표준편차(relative standard deviation, %RSD)로 판단하였다. 즉, 일내(intra-day)와 일간(inter-day) 시험을 통하여 실시하였다. 각각의 실험은 3가지 농도의 혼합표준용액을 3회 반복 실험을 통하여 얻는 결과의 상대표준편차를 구하여 평가하였다.
Results and Discussion1. DPPH 라디칼 소거능 활성감국과 레몬그라스의 DPPH 라디칼을 50% 소거하는데 필요한 시료의 농도(RC50)를 Table 1에 나타내었다. 실험결과, 감국 50% 에탄올추출물에서 48.32±1.07 µg/mL, 레몬그라스 50% 50% 에탄올추출물에서 48.51±1.44 µg/mL 로 나타났으며, 두 추출물을 혼합했을 때는 37.96±0.31 µg/mL 로 나타났다. 양성대조군으로 사용한 L-ascorbic acid (52.10±0.49 µg/mL)보다 단일 추출물일 때 약 1.1배, 혼합 추출물일 때 1.4배 더 강한 소거 활성을 나타내었다. 감국과 레몬그라스를 단독으로 사용하는 것 보다는 혼합물로 사용하는 것이 항산화 활성을 더욱 강화한다는 것을 알 수 있다. Ham et al. (2018) 이 산구절초, 자소엽, 찔레의 조합물에 관해 보고한 바와 같이, 산구절초나 찔레 단독으로 사용하는 것보다 자소엽과의 혼합물로 사용하는 것이 항산화 활성을 증강시킨다. 물론 자소엽의 DPPH 소거능이 매우 우수하여 상대적으로 활성이 약한 산구절초와 찔레의 활성을 증강시킨 점이 예상된다. 그러나 본 연구에서는 감국과 레몬그라스의 DPPH 소거능이 비슷하지만 동량 혼합에 의해 그 활성이 약 28% 증가되었으며 이는 두 소재의 항산화 활성을 나타내는 유효성분이 상호작용하여 상승효과를 나타낸 것으로 추론된다. 화장품 조성물로서 항산화 효능을 최대화하기 위해서 단일 추출물보다 복합추출물을 사용하는 것이 효과적일 것으로 사료 되며, 감국과 레몬그라스 외에도 선행 연구로 보고 한 소재들을 적절한 조합의 추출물로 사용할 때 그 효능이 더욱 극대화될 것이며, 각 소재의 항산화 활성과 조합 비율에 관한 연구가 더 필요하다고 사료 된다.
2. 지표 성분의 정성, 정량 분석문헌 조사 및 LC/MS 분석을 통하여(데이터 미 제시) 지표 성분들로 예상되는 물질들을 몇 가지 선택하여, HPLC 분석을 통하여 각 지표 성분들의 표준 검량선을 구하였다. Table 2에 나타낸 바와 같이, 검량선의 상관계수는 0.9999 이상이었으며 직선성을 나타내었다. 동시에 감국과 레몬그라스 내의 지표 성분들의 함량을 구하기 위해 HPLC 분석을 통해 각 지표 성분들의 함량을 구하였으며 그 결과를 Table 3에 나타내었다.
한편, 지표 성분의 기준은 함량이 많은 것을 선택하는 것이 바람직하나, 동시 분석의 전제 조건에서 가장 중요한 기준 중의 한 가지는 동시 분석하려는 소재들의 지표 성분이 HPLC 분석 과정에 각 피이크가 겹치지 않아야 한다는 것이다. 선행연구에서 LC/MS를 이용하여 폴리페놀 또는 플라보노이드 성분 중 감국의 각 성분의 함량을 분석한 결과, 가장 많은 함량을 차지한 것은 chlorogenic acid였으나, 레몬그라스 역시 chlorogenic acid가 상당량(감국의 chlorogenic acid 함유량의 1/2) 검출되어 각 추출물의 특이 성분으로 보기 어려워, 감국의 지표성분은 astragalin (AG)으로 선정하였다. 물론 레몬그라스에도 AG가 함유되어 있으나 분석 결과 감국의 AG 함유량과 비교하여 극히 소량(약 1/33)인 점을 고려하여 결정하였다. 레몬그라스의 경우는 p-coumaric acid (PA)를 지표 성분으로 선정하였으며 감국에는 PA가 상대적으로 매우 미량 들어 있었다. Table 3에 나타낸 바와 같이, 감국 50% 에탄올추출물에서 AG는 retention time 28.58 min에 검출되었으며 그 함량은 0.24 µg/mg 이었다. 레몬그라스 50% 에탄올추출물에서 retention time 18.48 min에 PA가 검출되었으며 그 함량은 1.55 µg/mg 이었다. 감국추출물에서의 AG의 HPLC 프로파일(Figure 1A)과 레몬그라스 추출물에서 PA의 HPLC 프로파일(Figure 1B), 지표 성분의 구조(Figure 1C)를 Figure 1에 나타내었다(Kim, 2016).
3. 동시분석 조건의 확립감국과 레몬그라스 각각의 지표성분인 AG와 PA를 0.1% formic acid가 함유된 water와 0.1% formic acid가 함유된 acetonitrile의 분석 조건을 확립하여 동시 분석을 진행하였다. Figure 2에서 볼 수 있듯이, AG는 212, 265, 346 nm에서 극대흡수파장을 나타냈으며, p-coumaric acid는 211, 226, 309 nm에서 극대흡수파장을 나타내었다. DAD 검출 파장은 225, 237, 248, 324에서 검출하였다. 지표성분들이 각각 28.60 min, 18.73 min에 모두 검출되는 것을 확인하였다.
4. 특이성(speciticity)
Figure 3에 감국과 레몬그라스 추출물의 혼합물(Figure 3A, 3B)과 표준품(Fig 3C, 3D)의 크로마토그램을 비교한 것을 나타내었다. Figure 3A는 AG 표준품의 분석 파장인 237 nm에서 혼합물의 피크이고 Figure 3B는 PA 표준품의 분석의 파장인 248 nm에서 혼합물의 피크이다. Figure 3C, 3D는 각각 AG 및 PA 표준품의 피크이다. 혼합물의 크로마토그램 중의 AG, PA 피크는 표준물질들의 retention time과 일치하였으며, UV 흡광도를 비교하였을 때 서로 일치하므로 추출물에 선정한 지표 성분인 AG와 PA가 존재한다는 것을 알 수 있다(Figure 3).
5. 직선성(Linearity), 검출한계(LOD) 및 정량한계(LOQ)Astragalin의 피크 면적에 대한 검량선은 0.5-2.5 µg/mL의 농도 범위에서 상관계수(R2)=0.9999의 직선성을 나타내었으며, PA는 0.1-1 µg/mL의 농도에서 상관계수(R2)=0.9999의 직선성을 나타내었다. AG의 검출 한계(LOD)는 1.20 ng/mL, 정량 한계는(LOQ)는 3.59 ng/mL이었으며, PA의 검출 한계(LOD)는 0.07 ng/mL, 정량 한계는(LOQ)는 0.22 ng/mL이다(Table 2).
6. 회수율(recovery)추출물에 지표 성분 표준물질의 서로 다른 3가지의 농도로 첨가한 후 측정한 회수율을 분석한 결과를 Table 4에 나타내었다. 추출물에 표준물질의 농도를 각각 1, 1.5, 2 µg/mL이 되도록 첨가하였을 때, 각 회수율(%)은 AG에서 117.52, 121.74, 117.78%였으며, 정확성(RSD%)은 각각의 농도에서 0.46, 0.07, 0.16%였다. PA에서는 각 농도에서 회수율(%)은 102.20, 102.90, 102.17%였으며, 정확성(RSD%)은 각각 2.57, 0.01, 0.33%로 나타났다.
7. 정확성(accuracy) 및 정밀성(precision)회수율을 통해 일내(intra-day)와 일간(inter-day) 정확성을 측정한 결과, 일내는 AG에서 108.48%, PA에서는 110.58%의 정확성을 나타내었고, 일간은 각각 107.39, 110.79%의 정확성을 나타내었다. 회수율은 식약처 가이드라인 기준치인 회수율 오차 20% 이내를 만족하였다. 직선성 범위 내에서의 일정한 3가지 농도에서의 정밀성을 측정한 일내(intra-day)와 일간(inter-day)의 시험결과, 일내는 AG에서 0.05%, PA에서는 0.53% 정확성을 나타내었고, 일간은 각각 0.06, 0.29%의 정밀성을 나타내었다. 이는 가이드라인 기준치인 상대표준편차 5% 이하를 만족하였다(Table 5).
Conclusion본 연구에서는 감국과 레몬그라스 에탄올 추출물을 활용한 천연 화장품 복합 조성물의 지표성분 표준화 및 다성분 동시분석법의 확립을 위해 각각의 지표 성분을 AG와 PA로선정하였고 HPLC-DAD를 사용하여 직선성, 정확성, 정밀성 등의 분석을 수행하였다. 먼저, 감국과 레몬그라스의 DPPH 라디칼 소거 활성을 평가했을 때, 감국의 50% 에탄올추출물은 RC50이 48.32±1.07 µg/mL, 레몬그라스 50% 에탄올추출물은 48.51±1.44 µg/mL로 나타났으며, 두 추출물의 1:1 조성물은 37.96±0.31 µg/mL로 나타났다. 각각의 추출물은 양성대조군으로 사용한 L-ascorbic acid (52.10±0.49 µg/mL)보다 약 1.1배 강했으며, 조성물은 1.4배 더 강한 소거 활성을 나타내었다. 감국에서 AG의 함량은 0.24 µg/mg, 레몬그라스에서 PA의 함량은 1.55 µg/mg로 확인되었고 식약처 가이드라인에 적합한 직선성, 정확성, 정밀성 분석을 확립하였다. 이상의 결과로 설정된 분석법은 천연 화장품 소재의 제조 관리 및 품질관리를 위한 중요한 자료로 사용 될 수 있을 것이라 사료되며, 향후, 감국과 레몬그라스의 단일 추출물 및 조성물을 이용하여 우수한 천연화장품 소재로 개발하기 위해서는 다른 생리활성을 추가로 분석할 필요가 있을 것이다.
Acknowledgements본 연구는 농림축산식품부의 재원으로 농림수산식품 기획평가원의 농림축산식품연구개발사업(과제번호: 317024054SB020)의 지원에 의해 이루어진 결과로 감사드린다. 또한, 감국과 레몬그라스 추출물을 공급해준 남원시 화장품산업지원센터에 감사드린다.
NOTESFigure 1.HPLC profile of 50% EtOH extract (CI or CC), and the str uctures of marker compounds.(A), HPLC profile of marker compound from the 50% EtOH extract of CI at 237 nm; (B), HPLC profile of marker compound from the 50% EtOH extract of CC at 237nm. In the HPLC profile of CI, AG (28.5 min) was detected but PA was not detected (18.5 min). Conversely, in the HPLC profile of CC, PA (18.5 min) was detected, but AG was not detected (28.5 min). To analyze the CI and CC extracts simultaneously, AG and PA were selected as the indicator components of CI and CC, respectively (despite being detected in small amounts). (C), Structures of the marker compounds AG and PA. CI, Chrysanthemum indicum L.; CC, Cymbopogon citratus; AG, astragalin, PA,p-coumaric acid.

Figure 2.UV spectra of standard maker compound and maker compound in CI and CC mixture.(A), UV spectrum of standard astragalin; (B) UV spectrum of astragalin from CI and CC mixture; (C), UV spectrum of standard p-coumaric acid m; (D), UV spectrum of p-coumaric acid from CI and CC mixture. CI, Chrysanthemum indicum; CC, Cymbopogon citratus.
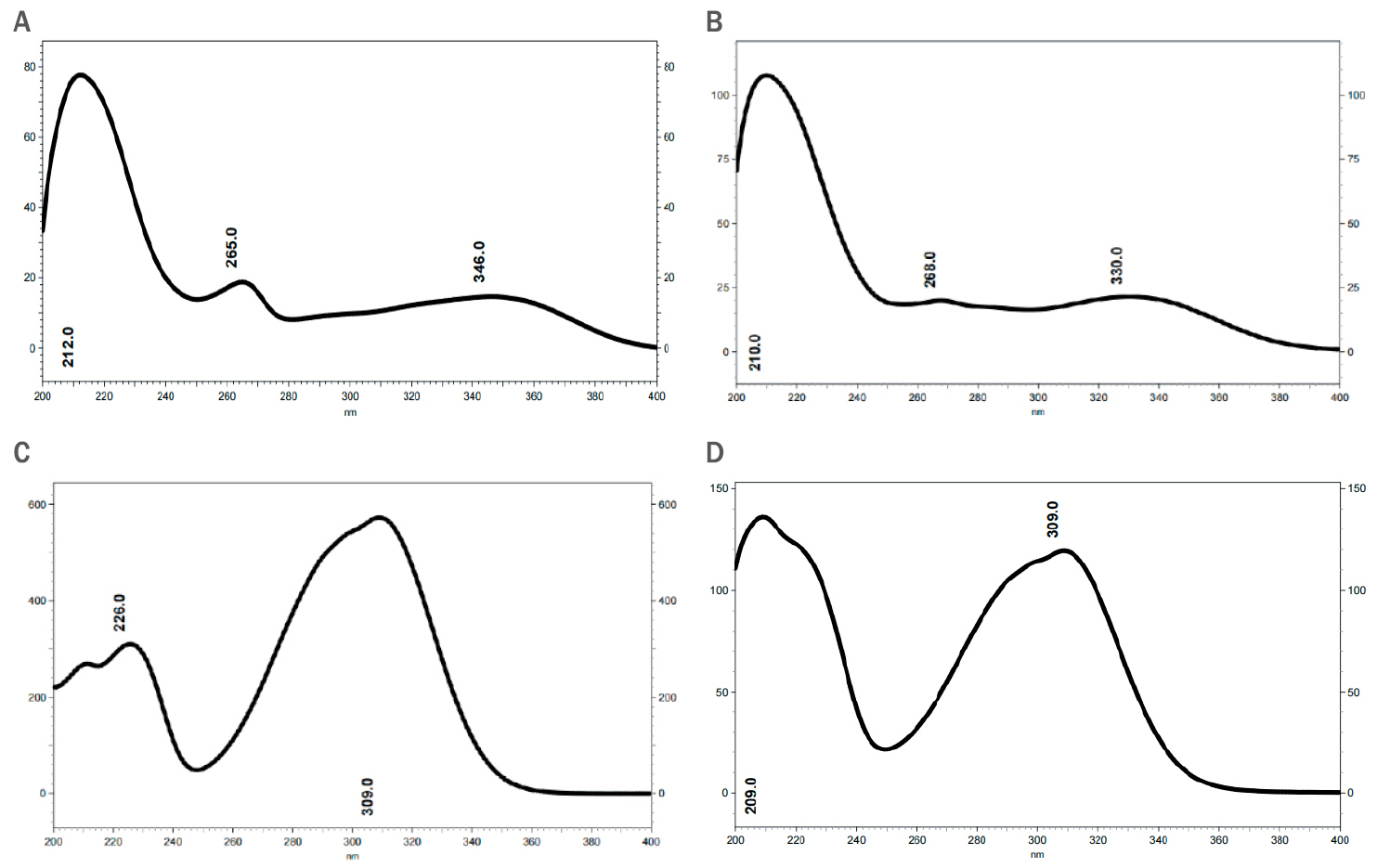
Figure 3.HPLC profile in simultaneous analysis ofthe CI and CC mixture.Panels (A) and (B) are chromatograms of mixed CI and CC profiled at 237 nm (the maximum absorption wavelength for AG analysis) and 248 nm (the maximum absorption wavelength for PA), respectively. Panels (C) and (D) are the HPLC profiles of the AG and PA standards, respectively. CI, Chrysanthemum indicum L.; CC,Cymbopogon citratus; AG, astragalin, PA, p-coumaric acid.
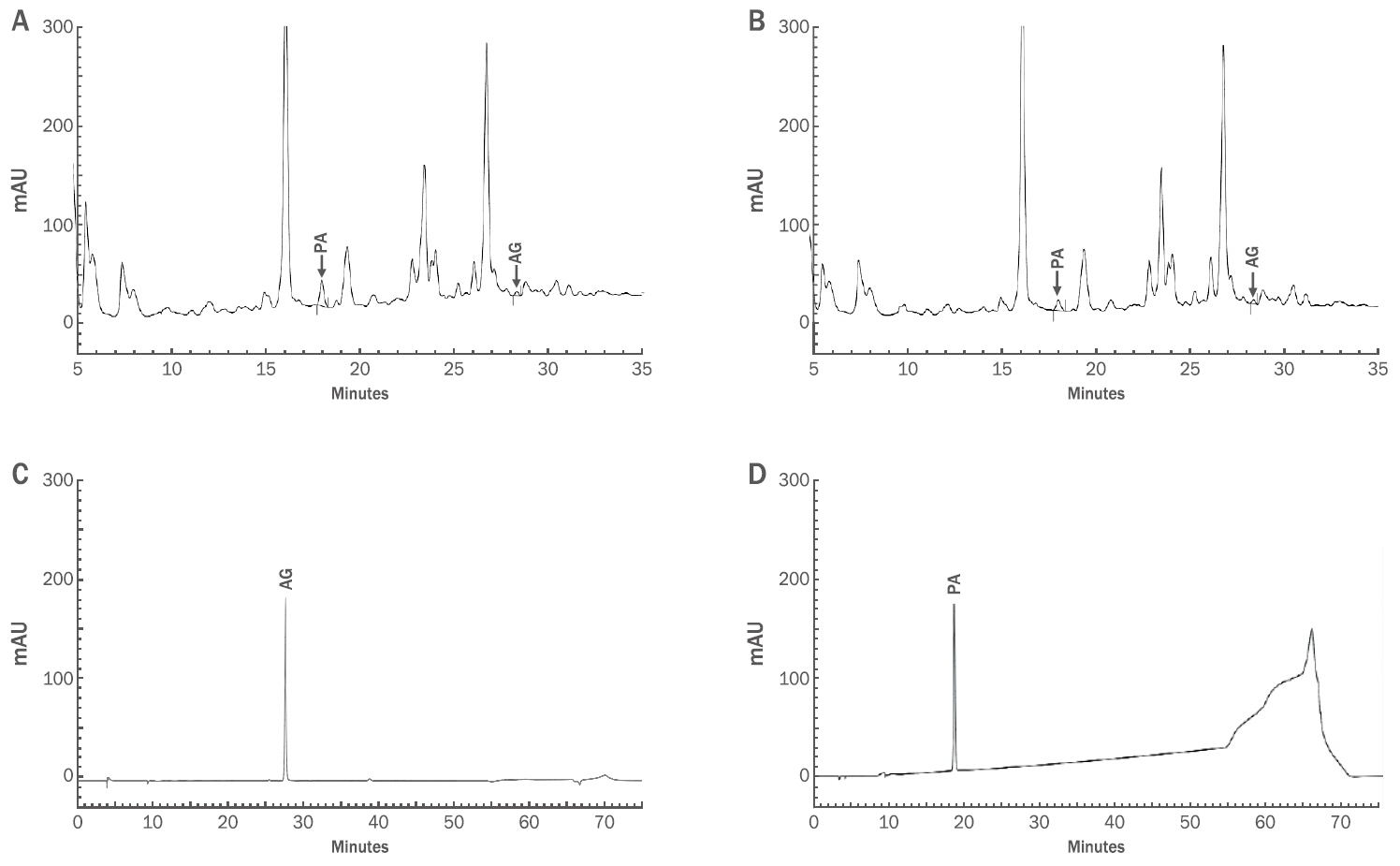
Table 1.RC50 values of DPPH scavenging activity
Table 2.HPLC calibration data for astragalin, p-coumaric acid. Table 3.Content analysis of the compounds in the extracts
Table 4.Recovery levels of astragalin and p-coumaric acid ReferencesAhn EM, Choi SA, Choi JY. HPLC analytical method validation of Aralia elata extract as a functional ingredients. Korean Journal of Food Preservation 24: 795-801. 2017.
Blois MS. Antioxidant determinations by the use of a stable free radical. Nature 181: 1199-1200. 1958.
Bhattacharya AK, Kaul PN, Rajeswara Rao BR. Effect of prolonged storage on the quality of lemongrass (Cymbopogon flexuosus (nees ex Stuud.) Wats.) essential oil. Journal of Essential Oil-Bearing Plants 1: 104-109. 1998.
Francisco V, Figueirinha A, Costa G, Liberal J, Lopes M. C, García-Rodríguez C, Batista MT. Chemical characterization and anti-inflammatory activity of luteolin glycosides isolated from lemongrass. Journal of Functional Foods 10: 436-443. 2014.
Ham HN, Shrestha AB, Kim JE, Leem JY, Lee TB, Yoo BW, Kim MS, Kim KS, Cha JS, Lee YM, et al. Simultaneous analysis of the compounds of natural cosmetic resource containing Chrysanthemum zawadskii, Perilla frutescens, Rosa multiflora and their anti-oxidative activity. Korean Journal of Pharmacognosy 49: 312-321. 2018.
Heo J. Donguibogam. Bubin Publisher. Seoul. pp577. 2017.
Hyun JM, Jo YJ, Kim YB, Park SM, Yoon KS, Lee NH. Antiinflammatory and anti-oxidative activities of flavonoids extracted from Dendranthema indicum flowers in Jeju Island. Journal of the Korean Applied Science and Technology 36: 1259-1267. 2019.
IPAI RIsearch. Market trend of the cosmetics industry and k-beauty overseas. Industry policy analysis institute. Seoul. pp58-106. 2017.
Jo YS, Ju SM, Hwang KH, Kim KS, Kim MS, Jeon BH. Inhibitory effect of Cymbopogon citratusethanol extracts on adipogenesis in 3T3-L1 preadipocytes. Journal of Physiology & Pathology in Medicine 33: 17-24. 2019.
Kim SJ, Park YM, Jung ST. Anticariogenic effects and inhibition of glucosyltransferase activity of Chrysanthemun indicum L. extracts. Journal of the Korean Society of Dietary Culture 20: 341-345. 2005.
Kim SG, Hong IP, Woo SO, Jang HR, Han SM. Anew analysis of p-coumaric acid and trans-cinnamic acid in propolis by UPLC. Korean Journal of Pharmacognosy 47: 186-191. 2016.
Kim YJ. Extracts of Chrysanthemum indicum Linne mediated regulation of MMP1 via JNK-AP1 pathway. Asian Journal of Beauty and Cosmetology 14: 399-405. 2016.
Kim TJ. Easy to find Korean herbal medicine (Korean medicine). Hyeonamsa. Seoul. pp76-77. 1998.
KFDA. Raw material standardization paper for health functional food developers. Korea Food and Drug Administration. Seoul. pp6-13. 2008.
Lee SM. Quantitative analysis of Ginsenosides using relative response factors from Ginsenoside Rf. Asian Journal of Beauty and Cosmetology 16: 211-219. 2018.
NIFDS. Drug validation guidelines. National Institute of Food and Drug Safety Evaluation. Seoul. pp1-19. 2015.
Park YM, Kim JI, Lee CH, Lim HJ, Seo EW. Effect of Dendranthema indicum extracts on cell and DNA damage induced by oxidative stress. Journal of Life Science 21: 1698-1704. 2011.
So YK, Hwang JY, Kim HW, Jo HN, Lee TB. Skin hydration and skin barrier effects of Cymbopogon ciratus and Perilla frutescens extracts. Journal of the Society of Cosmetic Science Korea 45: 225-235. 2019.
Woo JH, Shin SL, Lee HC. Antioxidant effect of 80% ethanol extracts obtained from three Dendranthema species. Korean Journal of Plant Resources 23: 47-53. 2010.
Yong YS, Lee SM, Byun NY, Sun SU, Kim MJ, Jang SW, Jang WS, Lee SY, Yim SH. Antioxidant activities and validation of analytical method of marker compounds in strawberry fruits from various cultivars. Korean Journal of Food Science and Technology 51: 517-523. 2019.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||