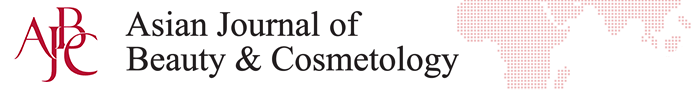Introduction
네일 서비스의 가장 기본은 네일 케어로, 이때 사용되는 네일 화장품은 큐티클 리무버이다. 큐티클 리무버는 큐티클을 연화시키기 위한 네일용 화장품으로 주요성분은 포타슘 하이드록사이드 (potassium hydroxide)와 소듐 하이드록사이드(sodium hydroxide)이다. 이 성분들은 큐티클 리무버에서 각질 연화의 목적으로 사용되며, 화장품의 pH를 강알칼리성으로 만든다. 네일케어 과정에서 큐티클 리무버는 큐티클 부위에 직접 도포하며 메탈푸셔를 이용하여 큐티클을 강하게 들어 올리고 니퍼로 큐티클 부위를 제거하면서 손톱 손상 및 큐티클 주변 피부의 손상이 필연적으로 일어난다(Baran, 2002; Hare & Rich, 2016).
이러한 부작용을 최소화하기 위해 보습과 영양 공급 효능이 있는 화장품 원료들이 추가된 저자극성의 큐티클 리무버 제품이 출시되고 있지만(Jefferson & Rich, 2012; Shim et al, 2019), 포타슘 하이드록사이드와 소듐 하이드록사이드의 함량 변화와 저자극성의 효능에 대한 정보는 찾아보기 어려운 실정이다. 또한 Environmental Working Group (EWG)'s Skin Deep에서조차 네일 샵에서 보편적으로 사용되는 네일 큐티클 리무버의 안전성에 대한 정보가 제한적이다. 즉, 저자극성 혹은 천연 큐티클 리무버 화장품이라고 광고하는 네일 화장품이 실제적으로 어느 정도 피부 손상을 방지하는지에 대한 유해성은 파악하기 어렵다.
네일 화장품의 유해성에 관련한 선행연구로는 주로 에나멜, 아세톤 등에 집중되어 있며(Baran & André, 2005; Felzenszwalb et al, 2019; Iorizzo, 2007; McLain, 2008; Yun & Lee, 2017), 큐티클 리무버의 유해성에 관한 연구는 거의 존재하지 않는다. 따라서 이 연구에서는 시판되고 있는 네일 전문 화장품 중 샵에서 가장 일반적으로 사용되고 있는 3개의 큐티클 리무버를 선정하여 세포독성에 대한 화장품 안전성을 평가하였다. 안전성 평가는 큐티클 리무버가 적용되는 실제적 환경을 고려하여 인체에서 채취한 조갑기질세포(nail matrix cell)와 인체각질형성세포(human skin keratinocyte cell, HaCaT), 인체피부섬유아세포(human skin fibroblast cell, HS68)를 사용하여 큐티클 리무버의 세포독성 정도를 평가하였다.
Methods
1. Material
1) Cuticle remover
시판되는 네일 큐티클 리무버의 안전성 평가를 위해 네일 샵에서 일반적으로 사용되는 대표적인 제품 3개를 선정하였다. 선정제품은 수입화장품인 Universal (VA, USA) 사의 Blue cross 제품과 국내화장품인 Cuore (Incheon, Korea) 사의 Zero cleanser, Bandi (Seoul, Korea) 사의 Flower vita cuticle care이다.
2) Reagent
세포의 배양을 위해 HBSS, Antibiotic은 BRL (ON, Canada) 사의 제품을 사용하였으며, fetal bovine serum (FBS), Dulbecco's Modified Eagle's Medium (DMEM), Keratinocyte growth medium (KGM), Iscove's Modified Dulbecco's Medium (IMDM)은 Gibco BRL (Rockville, USA)사의 제품을 사용하였다. 세포 생존율 측정을 위해 CellTiter 96® Non-Radioactive Cell Proliferation Assay (MTT, Dye Solution & Stop Solution)는 Promega (Madison, USA)사의 제품을 사용하였다.
2. Primary nail matrix cell culture
조갑기질세포의 배양을 위해 사람의 조갑기질 일부를 조갑 수술을 통해 채취하였다(연구승인번호: WKUH-2020-10-004). 채취한 조갑기질을 HBSS에 2x Antibiotic-Antimycotic을 첨가하여 3회 세척하였다. 조직을 배양접시로 옮겨 collagenase type IV (DMEM 3 mg/mL)를 조직이 잠길 정도로 놓은 후 CO2 배양기에 2-3 h 동안 방치하고 조직이 완전히 묽은 상태로 변할 때까지 기다린다. 이후 조직을 700 rpm으로 5 min 동안 원심분리하여 상측액 제거 후 펠렛을 DMEM에 녹여 37℃, 5% CO2 배양 조건에서 배양하였다.
3. Assessment of cell viability
1) Cell culture
일차 배양된 조갑기질세포는 DMEM 배지에 10% FBS, 1x antibiotics를 첨가하여 37℃, 5% CO2의 조건에서 배양하였다(Yoo et al, 1997). HaCaT 세포주는 Addex Bio (Addex Bio, USA)에서 분양받아 사용하였다. 분양받은 세포는 KGM 배지에 10% FBS, 1x antibiotics를 첨가하여 37℃, 5% CO2의 조건에서 배양하였다. HS68 세포주는 ATCC (USA)에서 분양받아 사용하였다. 분양받은 세포는 IMDM 배지에 10% FBS, 1x antibiotics를 첨가하여 37℃, 5% CO2의 조건에서 배양하였다.
2) MTT assay
네일 큐티클 리무버 화장품의 세포독성을 평가하기 위해 조갑기질세포(nail matrix cell), 인체각질형성세포(keratinocyte cell line, HaCaT), 인체피부섬유아세포 (human fibroblast skin cell, HS68)를 사용하여 MTT assay (3-(4, 5-dimethylthiazol-2-yl)-2, 50diphenyltetrazolium bromide)를 수행하였다. 배양된 조갑기질세포와 HaCaT, HS68을 96 well에 각 well 당 1×104 cells/mL로 분주 후 37℃, 5% CO₂조건에서 24 h 배양하였다(Yoo et al, 1998). 배양 후 배양액을 제거하고 농도별로 희석한 시료를 각 well 당 100 μL 씩 24 h 동안 반응시켰다. 이 후 상층액을 제거하고 PBS로 세척하여 시료의 색상이 흡광도에 영향을 미치지 못하도록 하였다. 각 well에 배양액 100 μL과 dye solution 15 μL을 첨가하여 Incubator에 4 h 동안 반응시켰다. 그 후 stop solution 100 μL씩 첨가하여 1 h 동안 반응시킨 후 ELISA reader (Spectramax M3; Molecular Devices, USA)에서 570 nm의 파장으로 흡광도를 측정하였다.
Results
큐티클 리무버 화장품의 세포독성을 평가하기 위해 조갑기질세포를 사용하여 세포 생존율을 측정한 결과는 Figure 1과 같다. 큐티클 리무버 화장품 시료의 농도가 높아질수록 세포 생존율은 감소하였다. Blue cross의 경우, 1 μg/mL 농도를 처리하였을때 조갑기질세포의 생존율이 101.33 (±1.53)%였고, 1.75 μg/mL에서는 86.33 (±5.78)%로 세포 생존율이 약간 낮아졌지만 80% 이상으로 나타났다. 그러나 2.5 μg/mL의 농도에서 세포 생존율이 0.67 (±0.58)%로 세포가 모두 사멸하였다(p<0.001). Zero cleanser의 경우, 1 μg/mL 농도에서 세포 생존율은 101.33 (±1.00)% 였고, 1.75 μg/mL 농도에서 74.00 (±2.65)%로 낮아져 control과 유의한 차이가 나타났다 (p<0.05). 또한 2.5 μg/mL 농도에서 5.00 (±1.73)%로 세포 생존율이 급격하게 낮아졌으며 10 μg/mL 농도에서는 세포가 모두 사멸하였다. Flower vita는 0.5 μg/mL, 1 μg/mL, 1.75 μg/mL, 2.5 μg/mL, 10 μg/mL, 20 μg/mL의 농도에서 약 100%에 가까운 세포 생존율을 유지하였으나 25 μg/mL의 농도에서 55.67 (±1.53)%으로 낮아져 세포독성을 확인하였다(p<0.001).
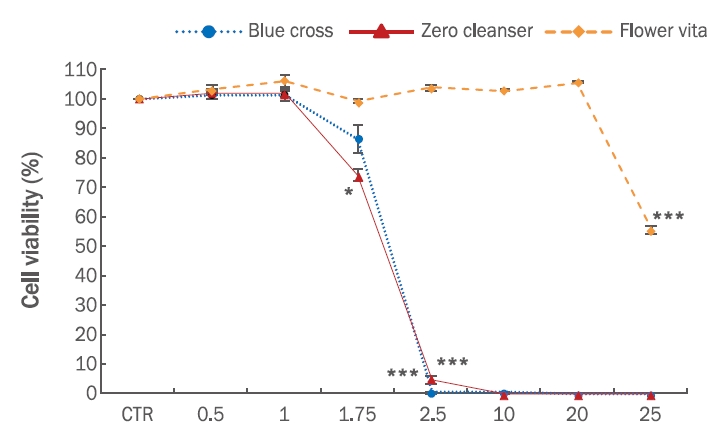
인체각질형성세포를 이용하여 큐티클 리무버의 세포독성을 측정한 결과는 Figure 2와 같다. Blue cross의 경우, 0.5 μg/mL 농도에서 65.67 (±3.51)%의 세포 생존율을 보여 70%이하의 세포 생존율로 세포독성을 확인하였다(p<0.01). 1.0 μg/mL, 1.75 μg/mL, 2.5 μg/mL, 10 μg/mL, 20 μg/mL로 농도가 증가함에 따라 세포 생존율이 감소하였으며 20 μg/mL의 농도에서 모든 세포가 사멸하였다. Zero cleanser 제품에서도 0.5 μg/mL 농도에서 62.33 (±4.73)%의 세포 생존율을 보여 세포독성을 확인하였다(p<0.01). 1.0 μg/mL 농도에서는 24.00 (±3.46)%로 나타났고 1.75 μg/mL 농도 이후 모든 세포가 사멸하였다. Flower vita 제품은 0.5 μg/mL 농도에서 세포 생존율이 93.67 (±1.53)%로 나타났고, 1.0 μg/mL 농도에서 89.67 (±1.53)%, 1.75 μg/mL에서 86.00 (±1.73)%, 2.5% μg/mL에서 85.33 (±2.52)%, 20 μg/mL에서 71.66 (6.35)%로 나타나 20 μg/mL까지의 농도에서 70% 이상의 세포 생존율을 확인하였다. 그러나 25 μg/mL에서 세포 생존율이 7.00 (±1.00)%로 감소하여 세포독성을 확인하였다.
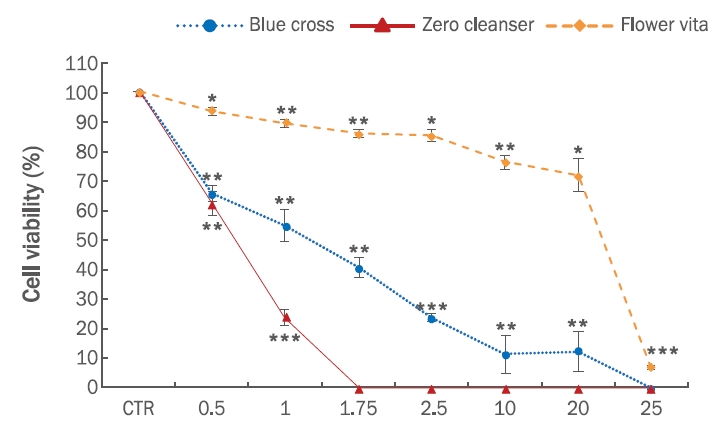
인체피부섬유아세포를 이용하여 큐티클 리무버의 세포독성을 측정한 결과는 Figure 3과 같다. Blue cross의 경우, 0.5 μg/mL 농도에서 HS68의 세포 생존율은 90.00 (±4.00)%였고, 1.0 μg/mL 농도에서 88.33 (±2.08)%였다. 1.75 μg/mL를 처치하였을 때 77.33 (±8.08)%로 농도가 증가할수록 세포 생존율이 낮아졌으며, 2.5 μg/mL 농도에서 40.67 (±2.08)%로 세포독성을 확인하였다. 또한 10 μg/mL 이상의 농도에서는 세포가 거의 사멸하였다. Zero cleanser의 제품을 HS68에 1.0 μg/mL로 처치하였을 때 95.67 (±0.58)%의 높은 세포 생존율을 보였으나 농도가 1.75 μg/mL에서는 69.67 (±8.33)%로 세포 생존율이 70% 이하로 나타났다(p<0.05). 또한 2.5 μg/mL의 농도에서는 30.33 (±1.53)%로 감소하였고 10 μg/mL 이하의 농도에서 세포가 모두 사멸하였다. Flower vita의 경우, 0.5 μg/mL, 1 μg/mL, 1.75 μg/mL의 농도에서 100%에 가까운 세포 생존율을 유지하였고 2.5 μg/mL, 10 μg/mL, 20 μg/mL의 농도에서도 90% 이상의 높은 세포 생존율이 나타났다. 25 μg/mL의 농도에서부터 7%로 낮아져 세포독성을 확인하였다.
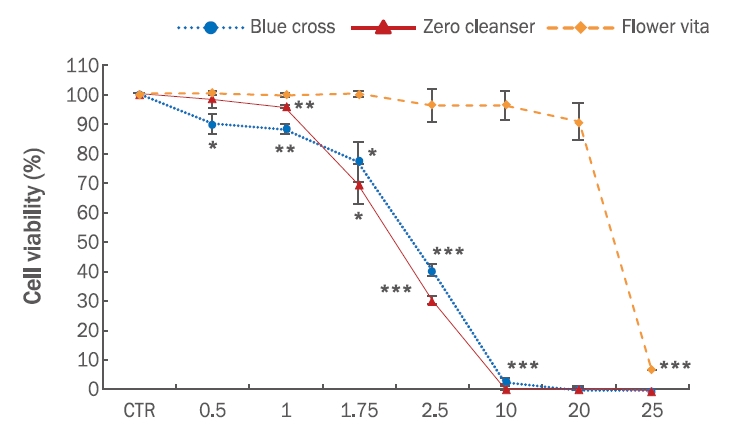
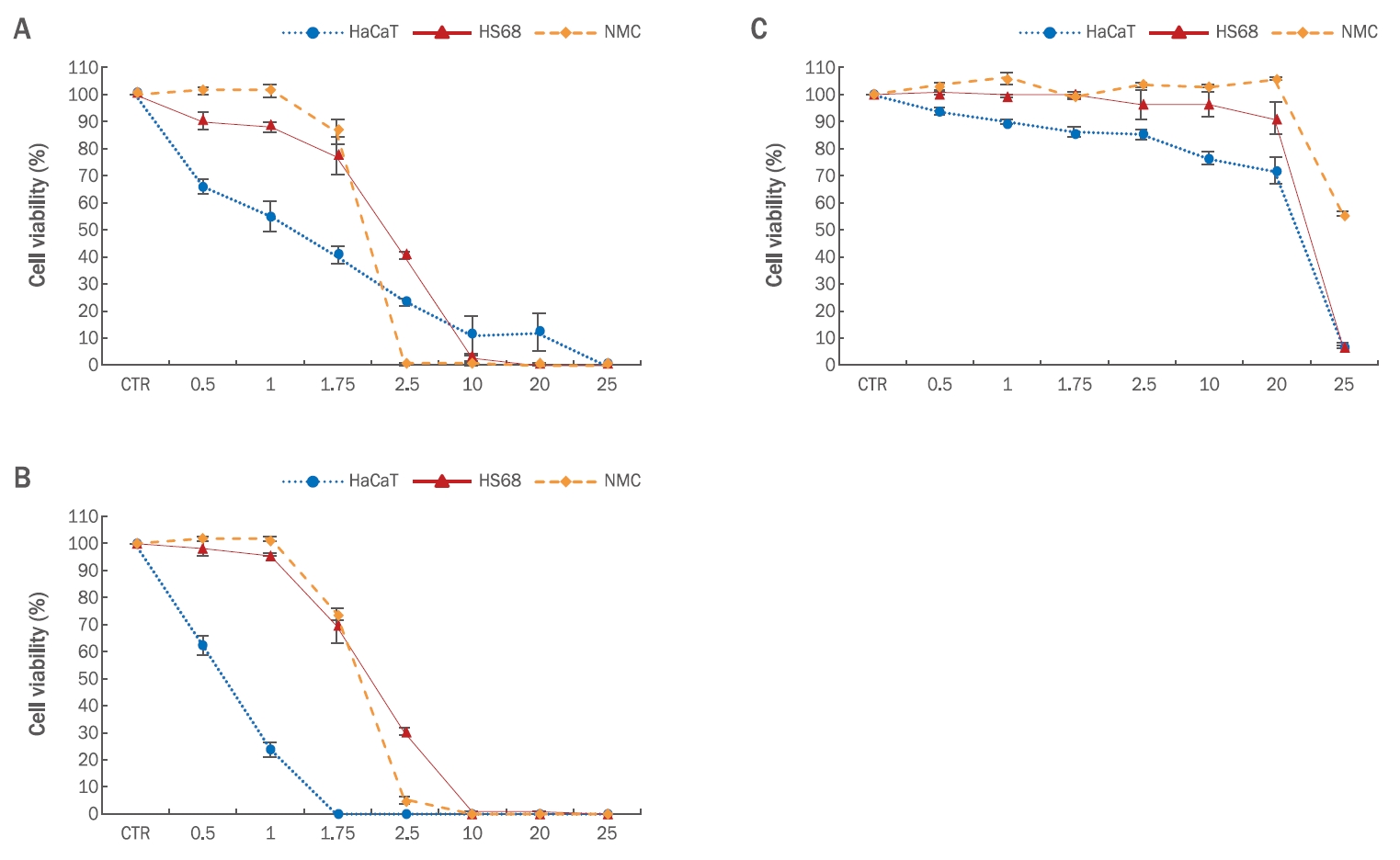
큐티클 리무버 제품을 조갑기질세포, 인체피부섬유아세포, 인체각질형성 세포를 이용하여 세포독성을 평가하였을 때 세포에 따라 동일 제품에서도 각각 세포 생존율의 차이가 나타났다(Figure 4).
Blue cross 제품을 조갑기질세포, 인체피부섬유아세포, 인체각질형성 세포를 이용하여 세포독성을 평가하였을 때 0.5 μg/mL, 1 μg/mL, 1.75 μg/mL에서는 조갑기질세포의 세포 생존율이 가장 높게 나타났으며 다음으로 인체피부섬유아세포, 인체각질형성세포 순으로 나타났다. Blue cross 제품 농도가 2.5 μg/mL에서는 조갑기질세포가 모두 사멸하였으나, 반면 인체피부섬유아세포의 생존율은 40.67 (±2.08)%로 가장 높게 나타났다. 10 μg/mL 이상의 농도에서는 조갑기질세포와 인체피부섬유아세포의 경우 세포가 모두 사멸하였으며, 인체각질형성세포 또한 약 10 % 정도의 세포 생존율을 보여 세포가 거의 사멸하였음을 알 수 있었다(Figure 4A).
Zero clenser 제품을 조갑기질세포, 인체피부섬유아세포, 인체각질형성세포를 이용하여 세포독성을 평가한 결과를 살펴보면(Figure 4B), 0.5 μg/mL, 1 μg/mL, 1.75 μg/mL 농도에서 조갑기질세포와 인체피부섬유아세포는 70%에 가까운 세포 생존율을 보인 반면 인체각질형성세포에서는 가장 저농도의 0.5 μg/mL에서 62.33 (±4.73)%의 세포 생존율을 보였다. 2.5 μg/mL 농도에서는 모든 세포의 세포 생존율이 급격히 감소였다. Zero clenser 제품의 경우 인체각질형성세포에서의 세포 생존율이 다른 제품에 비해 현저히 낮게 나타나 다른제품에 비해 인체각질형성세포에 대한 세포독성이 있음을 확인하였다.
조갑기질세포, 인체피부섬유아세포, 인체각질형성세포를 이용하여 Flower vita 제품의 세포 생존율을 평가한 결과는 Figure 4C와 같다. Flower vita 제품은 0.5 μg/mL에서 20 μg/mL 농도까지 조갑기질세포, 인체피부섬유아세포, 인체각질형성세포 모두 약 70% 이상의 세포 생존율을 보여 세포독성에 대한 안전성을 확인할 수 있었다. 25 μg/mL 농도에서는 인체피부섬유아세포와 인체각질형성세포에서 세포가 거의 사멸하였으며, 조갑기질세포에서는 55.67 (±1.53)%의 세포 생존율을 보였다.
Discussion
큐티클 리무버를 손톱 주변에 사용하면 조갑을 둘러싸고 있는 표피에 일차적으로 직접 접촉하고 표피를 통해 흡수된 큐티클 리무버는 진피에도 영향을 미친다. 또한 조갑을 형성하는 조갑기질에도 흡수되어 생물학적 효과가 나타날 가능성이 있다. 따라서 이 연구에서 시판 큐티클 리무버의 안전성 평가를 위해 배양조갑기질세포, HaCaT, HS68 등의 세 종류의 세포를 사용하였다.
네일 화장품의 부작용에 관한 선행연구는 여러 가지 종류의 네일 화장품이 피부에 미치는 영향을 in vivo와 in vitro를 통해 분석한 연구가 보고되고 있다(Mendelsohn et al., 2016; Taofiq et al., 2019). 특히 세포독성 분석법이 화장품 개발 단계에서 독성 물질 여부를 확인하는 실험 법이 보고되고 있으며(Hamid et al, 2004; Kim et al, 2019a; Ryu et al, 2019), 세포독성평가는 인체의 유해성을 확인할 수 있는 적용이다(Tomankova et al., 2011; Kim et al., 2019b).
따라서 이 연구에서는 시판 큐티클 리무버 화장품이 피부 및 손톱 기질에 미치는 영향을 분석하기 위해 세포독성 분석법 중 MTT assay를 시행한 결과 배양조갑기질세포, HaCaT, HS68 세포 주 모두에서 농도 의존적으로 세포 생존율이 감소하는 결과를 보였다.
조갑기질세포를 이용한 세포독성에 관한 연구 결과는 매우 드물다. 인체에서 조갑기질 일부를 수술적으로 채취한다는 것이 매우 어렵기 때문이다. 조갑기질에 손상이 일어나면 조갑에 변형이 생기는 심각한 후유증이 나타날 가능성이 높다. 항진균제가 조갑기질세포의 생존에 미치는 영향을 보고한 보고가 있지만 네일 화장품 관련 연구에 적용하여 실험한 보고는 거의 없다(Yoo et al, 1998). 이 연구에서는 건강한 사람에서 채취한 조갑기질 일부를 가지고 일차배양을 시도하여 배양세포주를 확립하였다. 큐티클 리무버의 세포독성은 배양조갑기질세포와 HS68 세포주에서 유사한 결과가 나타났지만 HaCaT 세포주에서는 배양조갑기질세포와 HS68 세포에 비해 독성효과가 상대적으로 강한 것으로 측정되었다. 이러한 세포독성 효과의 차이는 큐티클 리무버가 본질적으로 가지고 있는 약리학적 특성과 함께 조갑기질세포의 생물학적 특성에서도 기인한다고 볼 수 있다.
Conclusion
이 연구에서는 시판 큐티클 리무버 화장품 중 가장 일반적으로 사용되는 Blue cross, Zero cleanser, Flower vita cuticle care의 세 제품을 선정하여 조갑기질세포, 인체각질형성세포, 인체피부섬유아세포를 이용하여 제품에 대한 세포 독성을 평가하였다.
세포독성 측정 결과, 세 가지 제품 중 Flower vita 제품이 조갑기질세포, 인체각질형성세포, 인체피부섬유아세포 모두 20 μg/mL 농도에서 70% 이상으로 가장 높은 세포 생존율을 보였다. 이 결과를 통해 Flower vita 제품이 조갑과 이를 둘러싸고 있는 인체 조직에 가장 손상을 적게 주는 것을 알 수 있었다. 그러나 인체각질형성세포에서는 세 가지 큐티클 리무버 모두에서 세포 독성이 강한 것으로 측정되었다. 이러한 차이는 큐티클 리무버의 구성 성분이 세포에 미치는 생물학적 특성에서 기인하는 것으로 사료된다.
결론적으로 Flower vita 제품이 세포 독성 측면에서 가장 안전한 제품임을 알 수 있었다. 큐티클 리무버 화장품의 경우 조갑과 주위 피부에 흡수되는 제품의 안전성을 측정하기 위해서 조갑기질세포에 대한 독성도 함께 측정해야 신뢰할 만한 결과로 인정받을 수 있을 것이다. 따라서 조갑기질세포 일차배양법과 세포독성 측정법은 조갑의 손상을 객관적으로 평가할 수 있는 유용한 방법으로 활용이 가능할 것이다.
이 연구는 배양이 어려운 인체 조갑기질세포의 일차배양법을 확립하여 제시하였으며, 시판 큐티클 리무버 화장품에 대한 세포독성 평가 결과를 객관적으로 제시하였습니다. 이를 기반으로 저자극의 안전성이 확보된 큐티클 리무버 화장품의 개발이 후속되어야 할 것으로 사료됩니다.