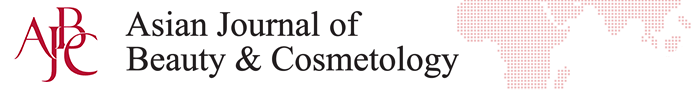울금 추출물의 피부미용식품 소재로서의 기능성 평가
요약
목적
생강과에 속하는 다년생 초본식물 울금(Curcuma longa L.)에 대한 항산화 및 항암 등의 연구가 비교적 다수 수행되었으나, 피부건강과 관련한 연구는 상대적으로 미미한 실정이다. 따라서, 본 연구에서는 국내 진도산 울금 물 추출물(water extracts of Curcuma longa L., CLE)의 B16F10 세포에서 멜라닌 생성 저해 활성 및 human skin fibroblasts (HSFs)에서 피부 섬유구조관련 유전자의 발현조절에 미치는 영향을 분석하여 울금 추출물의 미용기능식품 및 화장품 소재로서의 가능성을 평가하고자 하였다.
방법
B16F10, HSFs에서 CLE의 세포독성은 thiazolyl blue tetrazolium bromide (MTT) assay로 평가하였다. B16F10 세포에서 CLE의 멜라닌 생성 저해 활성은 세포의 배지에 용출된 멜라닌의 정량과 이미지 분석을 실시하였다. CLE가 HSFs 세포의 피부 섬유구조 관련 유전자의 발현에 미치는 영향은 reverse transcription-polymerase chain reaction (RT-PCR) 분석법을 통해 평가하였다.
결과
MTT assay를 통해 CLE의 농도는 B16F10 및 HSFs 세포에서 400 μg/mL 이하로 결정하였다. B16F10 세포에서 50, 100, 200, 400 μg/mL의 CLE 처리는 유의적으로 멜라닌 형성을 억제하였다. 또한 HSFs에서 10, 100, 200, 400 μg/mL의 농도로 CLE를 처리한 결과 procollagen1α1, procollagen1α2, elastin의 mRNA 발현수준을 현저히 증가시켰다.
결론
본 연구결과는 CLE를 이용하여 미백 및 피부섬유관련 유전자의 상향조절로 인한 피부탄력 증진에 효과가 있음을 확인하였으며 이후 미용기능식품 및 화장품 소재로서 충분히 활용될 수 있음을 시사한다
핵심용어: 울금, 피부, 멜라닌, 탄력, 미용식품
Abstract
Purpose
To test whether water extracts of Curcuma longa L. (CLE) have the potential as beauty food materials, the inhibitory effects of CLE on melanin accumulation in B16F10 cells and regulatory effects of CLE on the skin fibril-related genes in human skin fibroblasts (HSFs) were examined in this study.
Methods
Thiazolyl blue tetrazolium bromide (MTT) assay was used to evaluate the cytotoxicity of CLE in B16F10 or HSFs. Inhibitory effects of CLE on the melanin accumulation were evaluated by B16F10-eluted melanin content and image analysis. The expressions of skin fibril-related genes such as procollagen1α1, procollagen1α2, and elastin in HSFs were evaluated by reverse transcription-polymerase chain reaction (RT-PCR) analysis.
Results
Based on the cytotoxicity results, the concentrations of CLE were confirmed under 400 μg/mL in both B16F10 and HSFs. The cytotoxicity of B16F10 cells with CLE for 24 h was confirmed and CLE up to 400 μg/mL were used. The CLE from 50 to 400 μg/mL significantly inhibited melanin accumulation in B16F10 cells. The HSFs treated with CLE showed up-regulated skin fibril-related genes.
Conclusion
Those results show that CLE has benefits with skin-whitening and up-regulation of skin fibril-related genes, which means it could be used as an ingredient in beauty foods and/or cosmetic materials.
Keywords: Curcuma longa L., Skin, Melanin, Elasticity, Beauty food
中文摘要
目的
姜黄(Curcuma longa L.)属于生姜科的多年草本植物, 虽然对姜黄的抗氧化以及抗癌的先行研究比较多, 但皮肤健康相关的研究显然非常少。因此, 利用韩国国产姜黄水提取物(water extracts of Curcuma longa L., CLE), 在B16F10细胞中探讨黑色素抑制活性;在人皮肤成纤维细胞(human skin fibroblasts, HSFs)中, 探讨皮肤纤维相关基因的调控作用, 鉴定CLE的美容功效性食品和化妆品原料的应用可行性。
方法
在B16F10和HSFs细胞中CLE的细胞毒性, 利用thiazolyl blue tetrazolium bromide(MTT)assay法来评价。在B16F10细胞中, CLE的黑色素抑制活性, 通过细胞培养基中洗脱的黑色素含量和图像分析来进行测定。为鉴定CLE对皮肤纤维相关基因的调控作用, 通过reverse transcription-polymerase chain reaction(RT-PCR)方法来评价。
结果
在B16F10和HSFs细胞中, 利用MTT assay法确定CLE以后实验中采用浓度为400 μg/mL以下。在B16F10中, CLE分别以50、100、200、400 μg/mL浓度处理时, 明显抑制黑色素形成。在HSFs细胞中, CLE分别以10、 100、200、400 μg/m的浓度处理时, 其结果显示:procollagen1α1、procollagen1α2、elastin的mRNA表达水平具有浓度依赖性显著增加。结论:通过研究, 鉴定了CLE具有美白效能以及对皮肤纤维相关基因的调控, 具有增加皮肤弹力的效能。因此将来, CLE作为美容功效性食品和化妆品原料充分具有可行性。
关键词: 姜黄, 皮肤, 黑色素, 弹力, 美容食品
Introduction
피부는 크게 표피, 진피, 그리고 피하지방층으로 구성되어 있고, 이 중에서 표피는 피부의 가장 바깥쪽에 위치하며 다양한 외부환경에 의해 영향을 많이 받는 조직이다. 피부는 각질세포로 구성된 각질층에 의해 자외선 등을 비롯한 다양한 외부환경에 대한 방어 역할을 하고( Fisher et al., 2002; Kim et al., 2014), 체내의 수분과 전해질의 손실을 예방하는 역할을 한다( Elias, 1983; Feingold et al., 2007). 멜라닌은 표피의 하부층과 진피 사이에서 형성되며, 적정한 수준으로 존재할 때 자외선 등 외부의 자극에 대해 세포를 보호하는 이로운 역할을 수행한다. 또한 멜라닌은 형성되는 양과 종류에 따라 피부색, 눈동자, 그리고 머리카락 등의 색을 결정짓는 요인이기도 하다( Hill et al., 1997). 하지만 과도하거나 비정상적인 멜라닌 형성은 피부의 과 색소침착, 주근깨, 피부염증, 그리고 피부암 등을 야기한다고 알려져 있다( Urabe et al., 1994). 피부건강을 위협하는 탄력저하에 의한 주름의 발생은 피부의 진피조직의 변형에 의해 일어난다( Baumann, 2007). 진피층을 구성하는 단백질에는 대표적으로 콜라겐(collagen), 엘라스틴(elastin) 등이 있다. 콜라겐은 진피층의 90% 이상을 차지하고 있어 콜라겐의 과도한 분해 및 소실은 피부의 탄력을 저하시킨다. 이전의 연구에 따르면 외부자극에 의해 감소된 프로콜라겐(procollagen)에 의해 콜라겐의 분해를 증가시킴으로 탄력이 감소되고 주름 형성이 촉진되어 결과적으로 피부노화를 일으킨다고 알려져 있다( Brenneisen et al., 2002; Ito et al., 2010; Shephard et al., 2004). 따라서 이러한 콜라겐 및 엘라스틴 단백질을 유지하는 것은 피부의 건강한 탄력 및 주름 형성을 억제하는데 중요하다( Davies, 1987; Fantone & Ward, 1982). 최근 경제수준의 증가 등으로 인해 사람들의 피부건강에 대한 관심이 남녀 불문하고 크게 증가하고 있는 추세이다( Yaar & Gilchrest, 1998). 먹어서 아름다워진다는 이너뷰티(inner beauty) 시장의 급성장은 화장품 산업의 발달과 함께 식품산업에서도 중요하게 다뤄지고 있으며, 이와 관련하여 이너뷰티 소재를 탐색하고자 하는 다양한 연구가 수행되고 있다( Royer et al., 2013). 본 연구에서 사용한 울금( Curcuma longa L.)은 커큐미노이드(curcuminoid)라는 생리 활성 성분이 널리 알려져 있으며, 이와 관련된 다양한 연구가 보고되었다( Ammon & Wahl, 1991; Revathy et al., 2011). 울금의 생리학적 활성과 관련하여 다양한 보고가 있었으나( Shon & Kim, 2014), 피부건강 및 미용기능식품 소재로서의 울금에 대한 평가는 상대적으로 미비한 실정이다. 따라서 본 연구에서는 B16F10 세포에서 울금 추출물의 멜라닌 합성 저해를 통한 미백 활성을 평가하고, HSFs 세포에서 울금 추출물 처리가 피부의 탄력과 연관된 유전자인 procollagen1α1, procollagen1α2, elastin의 발현에 미치는 영향을 알아보았다. 이러한 결과를 바탕으로 울금 추출물이 미용기능성식품 소재로서의 이용 가능성에 고찰하고자 한다.
Methods
1. 실험 재료
본 실험에 사용된 국내 진도산 CLE는 ㈜삼진내추럴(Korea)에서 구입하여 사용하였다. CLE의 제조는 1 kg의 울금을 증류수 10 L에 희석하여 100±5℃에서 가열 및 추출한 후 1차 매쉬망 및 2차 필터를 통해 여과하였으며 최종 65 brix에 농축을 종료하여 제조되었다. MTT, 3-isobutyl-1-methylxanthine (IBMX), chloroform은 Sigma-Aldrich (USA)에서 구매하였으며, B16F10 및 HSFs 세포의 배양 등에 사용된 Dulbecco’s modified Eagle’s medium (DMEM), antibiotics (penicillin-streptomycin mixture), fetal bovine serum (FBS)은 Welgene (Korea)에서 구입하여 사용하였다. 그리고 isopropanol, dimethyl sulfoxide (DMSO)는 Junsei Chemical (Japan)에서 구입하였다. RT-PCR에 사용된 TRIzolⓇ은 Invitrogen™, Thermo Fisher Scientific (USA)에서, AccuPowerⓇ CycleScript RT PreMix는 Bioneer (Korea)에서, agarose는 Bio-Rad Laboratories (USA), 그리고 RNase-free water는 Welgene에서 구입하여 사용하였다. 본 연구에 사용된 B16F10 세포는 한국세포주은행(Korea)에서, HSFs는 American Type Culture Collection (USA)에서 분양 받아 이용하였다.
2. 세포독성 평가
B16F10 및 HSFs 세포에서 CLE의 세포독성을 평가하기 위해 MTT assay를 실시하였다. 세포는 12-well plate에 1×105 cells/mL 농도로 1 mL씩 분주하고 37℃, 5% CO2 환경에서 배양하였다. 100% 포화상태(confluent)가 되면 B16F10 세포에 10, 50, 100, 200, 400, 800 μg/mL의 농도로 CLE를 24 h 동안 처리한 후, phosphate buffered saline (PBS)에 녹여진 MTT 시약을 최종 200 μg/mL로 DMEM 배지에 희석하여 1 mL씩 분주하고 추가로 37℃에서 배양하였다(B16F10 30 min; HSFs 1 h). 반응이 끝나면 배지를 완전히 제거하고 DMSO를 각 well 마다 첨가하여(B16F10 400 μL; HSFs 300 μL), 보라색의 formazan을 용해한 후 96-well plate에 각각 분주하였고(B16F10 50 μL; HSFs 100 μL), microplate reader (VersaMax; Molecular Devices, USA)를 사용하여 570 nm의 흡광도에서 측정하였다. CLE를 처리하지 않은 B16F10 및 HSFs 세포의 흡광도 값을 대조군으로 하여 세포독성을 분석하였다.
3. 멜라닌 생성 저해 측정
CLE가 B16F10 세포의 멜라닌 생성에 어떠한 영향을 미치는지 알아보기 위하여 세포를 12-well plate에 1×105 cells/mL의 농도로 1 mL씩 분주한 후, B16F10 세포가 70% 포화상태가 되었을 때 500 μM IBMX를 72 h 동안 처리하여 멜라닌을 유도하고 CLE를 농도별로 10, 50, 100, 200, 400 μg/mL를 처리하여 37℃, 5% CO2 환경에서 배양하였다. 멜라닌 유도를 시키지 않은 B16F10 세포는 control (-), 멜라닌 형성을 유도하고 CLE를 처리하지 않은 B16F10 세포는 control (+)로 표기하였다. 멜라닌 유도 기간 동안 평균 3 times/day DMEM 배지를 갈아주었다. 유도가 끝난 후 B16F10 세포의 배지에 용출된 멜라닌을 96-well plate에 200 μL씩 넣어 microplate reader를 사용하여 405 nm의 흡광도에서 측정하여 CLE의 멜라닌 생성 저해 활성을 control (+)과 비교하여 평가하였다. 세포의 이미지는 위의 12-well plate를 CanoScan 9000F (Canon, Japan)으로 스캔하여 얻었다.
4. RT-PCR을 통한 mRNA 발현수준 평가
CLE 처리가 HSFs의 콜라겐 형성과 피부탄력 증진에 관여하는 유전자 발현에 어떠한 긍정적인 영향을 주는지 알아보기 위해 RT-PCR을 통한 mRNA 발현수준을 분석하였다. HSFs 세포를 12-well plate에 1×10 5 cells/mL의 농도로 1 mL씩 분주한 후, 10, 100, 200, 400 μg/mL 농도의 CLE로 2 h 동안 처리하였으며, TIRzol Ⓡ을 이용하여 총 RNA를 추출하였다. TRIzol Ⓡ 추출물에 100 μL의 chloroform을 넣은 뒤 15 s 동안 잘 혼합하여, 17,000 rpm에서 20 min 동안 원심 분리한 후 상층액을 획득하였다. 획득한 상층액에 250 μL의 isopropanol을 넣고 10 min 동안 상온에 방치한 다음 원심분리기를 이용하여 17,000 rpm에서 15 min 동안 RNA를 분리하였다. AccuPower Ⓡ CycleScript RT PreMix을 이용하여 분리된 RNA는 정량한 뒤 cDNA를 합성하였다. 또한 thermal cycler (T100™; Bio-Rad Laboratories)를 이용하여 합성된 cDNA는 RT-PCR을 수행한 후 mRNA 유전자 발현수준을 알아보기 위해 2% (w/v)의 agarose gel에 35 min 동안 전기영동 하여 유전자 발현을 분석하였다. 본 실험에 이용된 primer sequences는 Table 1와 같다. RT-PCR을 통한 RNA 발현수준을 평가한 것을 정량적으로 알기 위해 해당 밴드의 이미지 정량은 Image J 프로그램(National Institutes of Health, USA)을 사용하였다.
5. 통계분석
본 실험 결과의 데이터 통계는 3회 반복 실험하여 평균±표준편차를 이용하여 표현하였으며, Statistical Package for the Social Sciences (SPSS; IBM, USA) 프로그램을 이용하여 데이터 통계를 분석하였다. 각 그룹간의 유의성 정도를 평가하기 위해 일원배치 분산분석(one-way analysis of variance)법을 실시하였으며, 사후검증은 대조군과의 유의성 차이를 검증하는 Student’s t-test방법을 통해 실시하였다(p<0.05).
Results and Discussion
1. B16F10에서 CLE의 세포독성 평가
B16F10 세포에서 CLE의 세포독성을 평가하기 위하여 MTT assay를 실시하였다. B16F10 세포가 100% 포화상태가 되었을 때, CLE를 10, 50, 100, 200, 400, 800 μg/mL의 다양한 농도로 24 h 동안 처리한 결과, B16F10 세포의 생존율은 각각 99.30%, 94.56%, 97.80%, 79.08%, 86.43%, 75.92%인 것으로 나타났다( Figure 1). CLE 200 μg/mL과 800 μg/mL의 농도에서 유의적인 세포독성이 나타났으나, CLE 200 μg/mL에서의 세포 생존율은 80% 수준인 것을 감안하여 이후 실험은 CLE를 400 μg/mL 이하로 사용하였다.
2. B16F10 세포에서 CLE의 멜라닌 생성 저해 활성
CLE가 B16F10 세포의 멜라닌 생성을 억제하는지 알아보기 위하여 B16F10 세포가 70% 포화상태 되었을 때, 500 μM IBMX를 72 h 동안 처리하여 멜라닌 형성을 유도하고 같은 기간 CLE를 10, 50, 100, 200, 400 μg/mL의 유의적인 독성이 나타나지 않은 농도로 처리하였다. B16F10 세포의 배지에 용출된 멜라닌 함량을 측정한 결과 CLE를 10, 50, 100, 200, 400 μg/mL의 농도로 처리하였을 때 control (+) 대비 멜라닌의 함량은 64.28%, 20.69%, -3.22%, 18.37%, -3.78%인 것으로 나타났다. 특히 50, 100, 200, 400 μg/mL CLE 처리는 유의적으로 B16F10 세포의 멜라닌 형성을 억제하였다( Figure 2A). B16F10 세포에 축적된 멜라닌의 양을 이미지로 정성 분석하였을 때 위의 정량결과와 유사한 결과를 나타냈다. IBMX로 멜라닌 형성을 유도하지 않은 control (-) 대비 IBMX를 처리하여 멜라닌을 유도한 control (+)은 control (-)과 비교하여 다량의 멜라닌 형성이 관찰되었으며, CLE를 처리한 군에서는 control (+) 대비 멜라닌 함량이 감소된 것을 색 변화로 확인할 수 있었다( Figure 2B). 본 실험결과는 CLE가 멜라닌 형성을 억제하여 화장품 및 식품의 개발에 있어 효과적인 천연 미백소재로 활용될 수 있음을 시사한다. 이전의 연구에 따르면 1,000 μg/mL 울금의 에탄올 및 초임계 추출물이 각각 82.0%, 89.0%의 높은 티로시나아제(tyrosinase) 저해 활성을 나타낸다고 보고하였다( An et al., 2006). 멜라닌 형성과정에 있어 티로시나아제의 활성은 멜라닌 형성에 중요한 요소로 잘 알려져 있다( del Marmol et al., 1993). 따라서 본 실험에서 CLE의 B16F10 세포에서 멜라닌 억제 활성은 티로시나아제 효소의 저해에 의해 이뤄진 것으로 추측된다. 또한 Park et al. (2010)의 울금 추출물이 티로시나아제 저해 활성을 통해 멜라닌 형성을 억제할 수 있다는 선행연구는 본 실험의 결과를 뒷받침한다.
3. HSFs에서 CLE의 세포독성 평가
HSFs 세포에서 CLE의 세포독성을 평가하기 위하여 MTT assay를 실시하였다. HSFs 세포가 100% 포화상태가 되면 CLE를 10, 50, 100, 200, 400, 800 μg/mL의 농도로 24 h 동안 처리하였다. 그 결과 HSFs 세포의 생존율은 CLE를 처리하지 않은 대조군 대비 각각 100.99%, 95.84%, 93.28%, 93.08%, 90.94%, 86.80%로 나타났다( Figure 3). HSFs에서 CLE 400 μg/mL과 800 μg/mL 농도에서 유의적인 세포독성을 나타냈으며, 이후 실험에서는 400 μg/mL 이하의 CLE를 사용하여 실험을 진행하였다.
4. CLE 처리가 HSFs 세포의 procollagen1α1, procollagen1α2, elastin 발현에 미치는 영향
피부의 결합조직 단백질 중에는 콜라겐이 가장 큰 비율로 존재하며, 콜라겐 외에 엘라스틴과 같은 단백질이 존재하는 것으로 알려져 있다( Kim et al ., 2007). 새로이 합성되는 프로콜라겐은 fibrillogenesis 과정을 거치면서 콜라겐을 형성하게 되고 이로 인해 피부의 탄력을 구성하는데 기여하며, 또한 자외선에 의해서 진피층의 콜라겐 및 엘라스틴 단백질의 감소를 유발하여 피부의 탄력성 감소 및 주름 형성의 원인이 된다( Bateman et al ., 1996; Houben et al ., 2007). 진피는 대부분 fibroblasts로 구성되어 있으며, 세포외기질(extracellular matrix, ECM)을 생산하는 역할을 한다. 세포외기질에는 글리코스아미노글리칸(glycosaminoglycan)과 히알루론산(hyaluronic acid) 등의 다당류와 섬유상 단백질인 콜라겐, 엘라스틴 등이 존재한다. 따라서 본 연구에서는 CLE 처리가 피부조직의 형태를 유지하는 작용을 하는 콜라겐 및 피부조직의 탄력성과 관련성이 높은 엘라스틴의 발현에 미치는 영향을 확인하였다. CLE를 HSFs에 10, 100, 200, 400 μg/mL의 농도로 2 h 동안 처리한 후, procollagen1α1, procollagen1α2, elastin의 발현 정도는 RT-PCR을 통해 분석하였다. 그 결과, CLE 처리 농도가 증가할수록 HSFs에서 procollagen1α1, procollagen1α2, elastin의 발현수준이 증가함을 관찰하였다( Figure 4A– C). 그러나 본 연구에서 CLE 처리를 통해 프로콜라겐 및 엘라스틴의 발현증가에 대한 명확한 기전은 확인하지 못했으므로, matrix metalloproteinases 활성 및 활성산소종(reactive oxygen species)의 발생과 관련하여 CLE의 작용기전에 대한 추가 실험이 요구된다. 이전의 연구에 따르면 콜라겐 및 엘라스틴 펩타이드 혼합물(0.33%, w/w) 식이를 10주간 마우스가 섭취하였을 때 피부의 진피층에서 프로콜라겐의 합성이 유의적으로 증가하였으며, 이는 손상된 피부의 구조를 완화시켜 주름발생과 피부의 탄력증진에 기여할 수 있다고 보고되었다( Kim et al., 2009). 따라서, 본 연구에서의 CLE의 처리에 의한 procollagen1α1, procollagen1α2, elastin 유전자의 발현 증진은 진피층의 피부결합조직과 관련된 단백질인 콜라겐과 더불어 피부의 탄력 증진에 도움을 줄 수 있음을 보여주는 결과라고 생각된다.
Conclusion
본 연구에서는 울금 물 추출물(CLE)을 사용하여 B16F10 세포에서 멜라닌 생성 억제 활성을 통한 미백 활성을 평가하였으며, 또한 과도한 자외선으로 인해 주름이 생길 가능성이 있다는 보고에 따라 피부구조와 탄력에 연관성이 있는 procollagen1α1, procollagen1α2, elastin의 발현수준을 분석하기 위하여 HSFs를 활용하였다. 피부의 멜라닌 형성 및 탄력 증진 효능 평가를 위하여 각각의 세포모델에서 효능을 평가하였으며, 추후 3D 세포모델 확립을 통해 추가적인 흡수도 및 효능에 대한 검증이 요구된다. 또한 멜라닌 축적에 있어 B16F10 melanoma 세포가 아닌 normal melanocytes 모델을 통한 울금의 멜라닌 축적 억제 활성 역시 평가되어야 한다. 본 실험결과 B16F10 세포에서의 멜라닌 생성이 감소하였으며, 또한 HSFs 세포에서의 procollagen1α1, procollagen1α2, elastin의 발현수준을 증가시켰다. 따라서 CLE는 피부의 미백과 탄력에 효과를 줄 수 있는 소재로 활용될 수 있을 것이라 판단된다.
Acknowledgements
본 연구는 산업통상자원부와 한국산업기술진흥원의 “지역특화산업육성사업”(과제번호 R0005174)으로 수행된 연구결과 입니다.
Figure 1.
Effects of CLE on B16F10 viability.
B16F10 cells were treated with 10, 50, 100, 200, 400, and 800 μg/mL CLE for 24 h and cell viability was evaluated by MTT assay at 570 nm using the microplate reader. Statistical analysis was performed at *p<0.05 and **p<0.01 by t-test. The 200 and 800 μg/mL CLE affected to the cell viability of B16F10. Further experiment was conducted under 400 μg/mL of CLE. CLE, water extracts of Curcuma longa L.; Control, CLE untreated group; MTT, thiazolyl blue tetrazolium bromide.
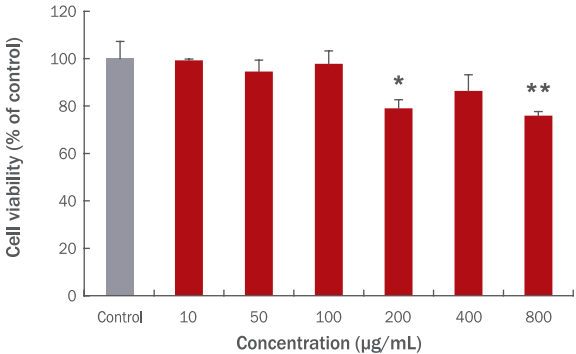
Figure 2.
Inhibitory effects of CLE on melanin accumulation of B16F10 induced by IBMX.
To confirm the effects of CLE on inhibition of melanin content, B16F10 cells were treated with 10, 50, 100, 200, and 400 μg/mL CLE and induced by 500 μM IBMX for 72 h. The cells treated with IBMX showed significant increased melanin content compared to control (-). Medium of the cells were collected and its melanin content was analyzed by microplate reader at 405 nm. The treatment of 50, 100, 200, and 400 μg/mL CLE significantly suppressed melanin accumulation of B16F10 (A). The changes of medium color were obtained using image scanner (B). Statistical analysis was performed at *p<0.05, **p<0.01, and ***p<0.001 by t-test. CLE, water extracts of Curcuma longa L.; IBMX, 3-isobutyl-1-methylxanthine; Control (+), IBMX treated group without CLE; Control (-), IBMX and CLE untreated group.
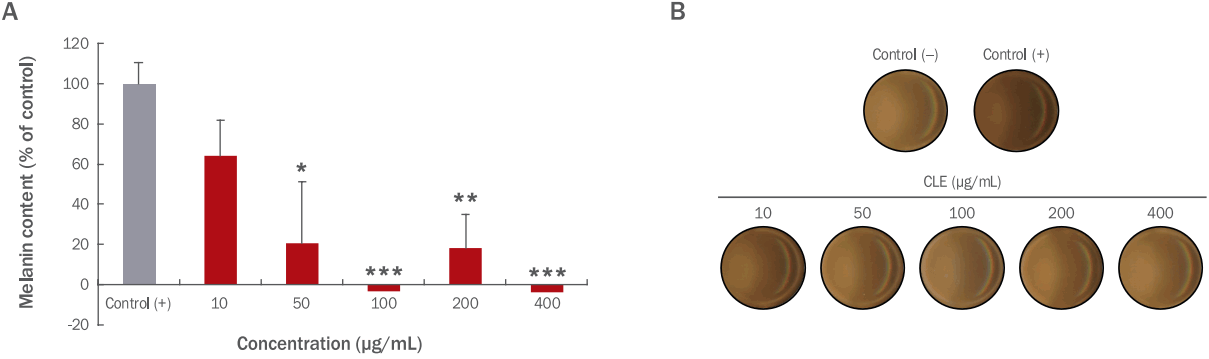
Figure 3.
Effects of CLE on HSFs viability.
HSFs were treated with 10, 50, 100, 200, 400, and 800 μg/mL CLE for 24 h and cell viability was evaluated by MTT assay at 570 nm using the microplate reader. The 400 and 800 μg/mL CLE significantly affected to the cell viability of HSFs. Further experiment was conducted under 400 μg/mL of CLE. Statistical analysis was performed at *p<0.05 by t-test. CLE, water extracts of Curcuma longa L.; Control, CLE untreated group; HSFs, human skin fibroblasts; MTT, thiazolyl blue tetrazolium bromide.

Figure 4.
Effects of CLE on mRNA expression of skin fibril-related genes in HSFs.
The HSFs were exposed to the 10, 100, 200, and 400 μg/mL CLE for 2 h. The mRNA expressions of skin fibril-related genes such as procollagen1α1 (A), procollagen1α2 (B), and elastin (C) were examined by RT-PCR analysis. The CLE treatment between 10 and 400 μg/mL up-regulated mRNA expressions of procollagen1α1, procollagen1α2, and elastin. Actin beta was used as a control. The mRNA expressions were quantified using Image J program. Each value of the graph corresponds to the percent concentrations divided by the amount of actin beta which is the control. Statistical analysis was performed at *p<0.05, **p<0.01, and ***p<0.001 by t-test. CLE, water extracts of Curcuma longa L.; Con, control (CLE untreated group); HSFs, human skin fibroblasts; RT-PCR, reverse transcription-polymerase chain reaction.
Table 1.
Primer sequences for RT-PCR analysis
|
Primer |
Forward (5'→3') |
Reverse (5'→3') |
|
Procollagen1α1 |
GTTGGGGGAGGGGTAGACAT |
AGAGGCCAGATGACCCTTCA |
|
Procollagen1α2 |
GCACCACTTGTGGCTTTTGA |
TACCACACCAAACTGCCCTT |
|
Elastin |
GAGGTTGCCCAACCAAAAGC |
TCAGAGGGGACTGTTTCGGA |
|
Actin beta |
GCAGGAGTATGAGAGTCCG |
AGGGACTTCCTGTAACAATGC |
References
Ammon HP, Wahl MA. Pharmacology of Curcuma longa. Planta Medica 57: 1-7. 1991.   An BJ, Lee JY, Park TS, Pyeon JR, Bae HJ, Song MA, Baek EJ, Park JM, Son JH, Lee CE, et al. Antioxidant activity and whitening effect of extraction conditions in Curcuma longa L. Korean Journal of Medicinal Crop Science 14: 168-172. 2006.
Bateman JF, Lamandé SR, Ramshaw JA. Collagen superfamily. In: Extracellular matrix, volume 2. In: Comper WD, ed. CRC Press. Boca Raton. pp22-67Z. 1996.
Baumann L. Skin ageing and its treatment. The Journal of Pathology 211: 241-251. 2007.   Brenneisen P, Sies H, Scharffetter-Kochanek K. Ultraviolet-B irradiation and matrix metalloproteinases: from induction via signaling to initial events. Annals of the New York Academy of Sciences 973: 31-43. 2002.   Chung JH. Photoaging in Asians. Photodermatology Photoimmunology & Photomedicine , 19: 109-121. 2003.  Davies KJ. Protein damage and degradation by oxygen radicals: Ⅰ. general aspects. The Journal of Biological Chemistry 262: 9895-9901. 1987.
del Marmol V, Ito S, Jackson I, Vachtenheim J, Berr P, Ghanem G, Morandini R, Wakamatsu K, Huez G. TRP-1 expression correlates with eumelanogenesis in human pigment cells in culture. FEBS Letters 327: 307-310. 1993.   Elias PM. Epidermal lipids, barrier function, and desquamation. Journal of Investigative Dermatology 80: 44s-49s. 1983.  Fantone JC, Ward PA. Role of oxygen-derived free radicals and metabolites in leukocyte-dependent inflammatory reactions. The American Journal of Pathology 107: 395-418. 1982.   Feingold KR, Schmuth M, Elias PM. The regulation of permeability barrier homeostasis. Journal of Investigative Dermatology 127: 1574-1576. 2007.   Fisher GJ, Kang S, Varani J, Bata-Csorgo Z, Wan Y, Datta S, Voorhees JJ. Mechanisms of photoaging and chronological skin aging. Archives of Dermatology 138: 1462-1470. 2002.   Fisher GJ, Wang ZQ, Datta SC, Varani J, Kang S, Voorhees JJ. Pathophysiology of premature skin aging induced by ultraviolet light. The New England Journal of Medicine 337: 1419-1428. 1997.   Hill HZ, Li W, Xin P, Mitchell DL. Melanin: a two edged sword? Pigment Cell & Melanoma Research 10: 158-161. 1997.  Houben E, De Paepe K, Rogiers V. A keratinocyte’s course of life. Skin Pharmacology and Physiology 20: 122-132. 2007.   Ito S, Itoga K, Yamato M, Akamatsu H, Okano T. The coapplication effects of fullerene and ascorbic acid on UV-B irradiated mouse skin. Toxicology 267: 27-38. 2010.   Kim B, Choi YE, Kim HS. Eruca sativa and its flavonoid components, quercetin and isorhamnetin, improve skin barrier function by activation of peroxisome proliferator-activated receptor (PPAR)-α and suppression of inflammatory cytokines. Phytotherapy Research 28: 1359-1366. 2014.   Kim JK, Lee JH, Yang MS, Seo DB, Lee SJ. Beneficial effect of collagen peptide supplement on anti-aging against photodamage. Korean Journal of Food Science and Technology 41: 441-445. 2009.
Kim N, Koo B, Lee S, Hwang E, So S, Do J. Effect of Korean red ginseng on collagen biosynthesis and MMP-I activity in human dermal fibroblast. Journal of Ginseng Research 31: 86-92. 2007.  Park EY, Hur SJ, Kim KY, Whang WK, Yang KS. Anti-oxidant and whitening effects of Curcuma longa L. Asian Journal of Beauty and Cosmetology 8: 111-120. 2010.
Revathy S, Elumalai S, Benny M, Antony B. Isolation, purification and identification of curcuminoids from turmeric (Curcuma longa Lby column chromatography. Journal of Experimental Sciences 2: 21-25. 2011.
Rittié L, Fisher GJ. UV-light-induced signal cascades and skin aging. Ageing Research Reviews 1: 705-720. 2002.   Royer M, Prado M, García-Pérez ME, Diouf PN, Stevanovic T. Study of nutraceutical, nutricosmetics and cosmeceutical potentials of polyphenolic bark extracts from Canadian forest species. PharmaNutrition 1: 158-167. 2013.  Seite S, Zucchi H, Septier D, Igondjo-Tchen S, Senni K, Godeau G. Elastin changes during chronological and photo-ageing: the important role of lysozyme. Journal of the European Academy of Dermatology and Venereology 20: 980-987. 2006.   Shephard P, Martin G, Smola-Hess S, Brunner G, Krieg T, Smola H. Myofibroblast differentiation is induced in keratinocyte-fibroblast co-cultures and is antagonistically regulated by endogenous transforming growth factor-β and interleukin-1. The American Journal of Pathology 164: 2055-2066. 2004.    Shon MS, Kim GN. Anti-oxidant and anti-obese activities of turmeric (Curcuma longa Lextract in 3T3-L1 cells. Asian Journal of Beauty and Cosmetology 12: 169-175. 2014.
Urabe K, Aroca P, Tsukamoto K, Mascagna D, Palumbo A, Prota G, Hearing VJ. The inherent cytotoxicity of melanin precursors: a revision. Biochimica et Biophysica Acta (BBA)-Molecular Cell Research 1221: 272-278. 1994.  Wenk J, Brenneisen P, Meewes C, Wlaschek M, Peters T, Blaudschun R, Ma W, Kuhr L, Schneider L, Scharffetter-Kochanek K. UV-induced oxidative stress and photoaging. Current Problems in Dermatology 29: 83-94. 2001.   Yaar M, Gilchrest BA. Aging versus photoaging: postulated mechanisms and effectors. Journal of Investigative Dermatology Symposium Proceedings 3: 47-51. 1998. 
|
|