Introduction
Melanin은 대부분 동물의 피부, 모발, 눈, 내이, 뼈, 심장, 뇌 등에 분포되어 있는 물질로 피부색을 결정한다(Alaluf et al., 2002; D’Mello et al., 2016). 이러한 melanin은 자외선으로부터 피부를 보호하고, 활성산소를 제거하는 역할을 하는 필수적인 생체 물질이다(Brożyna et al., 2016; Herrling et al., 2008). 하지만 비정상적인 melanin 축적은 기미, 주근깨, 모반, 검버섯과 같은 색소이상증을 일으킨다(Slominski et al., 2004). 때문에 melanogenesis 조절을 통해서 색소이상증을 조절할 필요가 있다. Melanogenesis는 기저층에 있는 melanocyte에서 일어나며 주로 tyrosinase에 의해서 조절된다(Hearing, 2011). Tyrosinase (EC 1.14.18.1)은 polyphenol oxidase (PPO)로 알려져 있으며 copper-containing monooxygenase enzyme으로 melanin 합성에 매우 중요하다(Parveen et al., 2010). 이러한 enzyme은 fungi, plant, animal 등에 다양하게 분포하고 있으며(van Gelder et al., 1997), L-tyrosine으로부터 melanin이 합성되는 초기과정인 3,4-dihydroxyphenylalanine (L-DOPA), dopaquinone이 합성되는 과정에서 중요하게 작용한다(Hearing, 2011; Slominski et al., 2005; Slominski et al., 2012). 이러한 tyrosinase는 melanocyte-stimulating hormone (α-MSH), adrenocorticotropic hormone (ACTH) 등과 같은 호르몬에 의한 신호전달기전에 의해서 microphthalmia-associated transcription factor (MITF)의 전사활성을 높이고, 이를 통해 tyrosinase를 발현시키게 된다(Brenner & Hearing, 2008; Costin & Hearing, 2007; Ha & You, 2016; Slominski et al., 2004). 때문에 melanogenesis의 조절은 관련 신호전달기전을 조절함으로써 가능하다.
Cnidium officinale Makino은 산형과 다년생 식물로 한국에서 천궁으로 불린다(Choi et al., 2002). 이러한 Cnidium officinale Makino은 아시아를 중심으로 오랜기간 동안 진통제, 항염제, 생리불순치료 등의 목적으로 전통의약제로 사용하고 있다(Hong et al., 2017). 또한 Cnidium officinale Makino의 주요성분인 phthalide 유도체들은 진정제, 항빈혈제, 항진균제, 이완제, 항보체 활성과 같은 다양한 효능을 가지고 있고, Cnidium officinale Makino 추출물 역시 혈액순환개선 및 염증성질환 억제의 효능이 있는 것으로 알려져 있다(Jang, 2017; Tahara et al., 1999; Wang et al., 1989). 특히, Higashi (1996)의 연구에서는 Cnidium officinale Makino가 이완작용에 효과적이고, 울혈과 염증을 억제하여 염증성질환으로 인한 가려움증을 완화할 수 있다고 알려져 있다. 또한 간암모델에서 Cnidium officinale Makino 추출물이 항암과 항전이 활성을 가진다는 것이 입증되었다(Haranaka et al., 1985; Hong et al., 2017; Onishi et al., 1998). 하지만 아직까지도 Cnidium officinale Makino가 피부에 존재하는 세포들에 대한 연구는 미비한 편이다. 때문에 본 논문에서는 Cnidium officinale Makino 추출물이 melanocyte에서 melanogenesis에 미치는 영향을 밝히고자 한다.
Methods
1. B16F10 mouse melanoma 세포배양
B16F10 mouse melanoma 세포는 한국세포주은행(Korean Cell Line Bank, Korea)에서 구매하였으며, Dulbecco’s modified Eagle’s medium (DMEM; Gibco, Thermo Fisher Scientific, USA)에 10% fetal bovine serum (FBS; Sigma-Aldrich, USA)와 10% penicillin (Gibco, 100 units/mL), 10% streptomycin (Gibco, 100 μg/mL)이 포함된 배지에 배양하였다.
2. Cnidium officinale Makino 추출물 제조
Cnidium officinale Makino을 1차 세척 후 60℃ 건조기(ON-50; Deahan Science, Korea)에서 완전히 건조를 한다. 건조된 Cnidium officinale Makino을 분쇄기(SMX-5800LM; Shinil, Korea)에 넣고 분말화하고, Cnidium officinale Makino 분말에 70% ethanol를 첨가하여, 60℃에서 30 min동안 추출한다. 추출하는 동안 20 kHz이상의 초음파(Ultrasonic cleaner 8891; Cole-Parmer, USA)를 주어서 추출효율을 높였다. 추출 후 남은 고형분을 여과지(Whatman No.2; GE Healthcare Life Sciences, USA)로 분리하고, 여과액을 감압농축기(EYELA N-3010; Tokyo Rikakikai, Japan)와 동결건조기(LP 10-30; Ilshin, Korea)로 건조하였다. 건조된 Cnidium officinale Makino 추출물은 다시 농도에 맞춰 dimethyl sulfoxide (DMSO; Biopure, Canada)로 녹였다.
3. 세포독성 측정
세포독성을 측정하기 위해서 3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT) assay를 진행하였다. 96 well plate에 3×103개의 B16F10 mouse melanoma 세포를 접종하고, 48 hr 후 추출물을 0–200 μg/mL로 처리하였다. 추출물이 처리된 세포를 48 hr 배양 후 0.5 mg/mL MTT (Sigma-Aldrich)로 처리하고 37℃에 1 hr 배양하였다. 1 hr 후 배지를 제거하고 생성된 MTT formazan을 DMSO로 녹여 595 nm에서 microplate reader (SpectraMax® i3x; Molecular Devices, USA)를 이용하여 흡광도를 측정하였다. 측정된 흡광도를 비교하여 세포독성을 표현하였다.
4. Melanin 생성량 측정
B16F10 mouse melanoma 세포에서의 melanin 함량 측정은 세포내의 melanin을 추출하여 흡광도를 측정하는 방법을 사용하였다. 60-mm cell culture dish에 2×105 개의 B16F10 mouse melanoma 세포를 접종하고 48 hr 배양하였다. 배양 후 세포에 melanin 생성 유도 물질인 α-MSH와 Cnidium officinale Makino 추출물을 처리하고 48 hr 배양하였다. 배양이 끝난 후 세포를 수확하여 PBS로 1회 세척하고 세포 수를 개수하였다. 각각의 샘플당 동일량의 세포로 분주하고 1 N sodium hydroxide (NaOH; Sigma-Aldrich) 100 μL를 첨가하여 95℃에서 15 min 세포를 용해하였다. 그 후 450 nm 파장에서 microplate reader를 이용하여 흡광도를 측정하여 melanin 함량을 확인하였다.
5. Tyrosinase 활성 측정
Tyrosinase 활성 측정은 0.1 M sodium phosphate buffer (pH 7.4)에 2 mM L-Dopa (Sigma-Aldrich)와 100 unit mushroom tyrosinase (Sigma-Aldrich) 또는 cell lysate 넣고 반응하여 측정하였다. Tyrosinase의 직접적인 저해효과를 보기 위해서 mushroom tyrosinase를 이용하였고, 간접적인 저해효과를 보기 위해서 cell lysate를 이용하였다. Cell lysate는 추출물을 처리한 세포를 1% Triton X-100 (Biopure), 150 mM sodium chloride (Biopure), 50 mM HEPES (pH 7.5, Biopure), 5 mM EDTA (Biopure)가 첨가된 lysis buffer를 이용하여 세포를 용해하였다. 반응은 37℃에서 30 min 반응하였으며, 반응을 통해서 합성된 melanin은 450 nm 파장에서 microplate reader를 이용하여 흡광도를 측정하여 확인하였다. Cell lysate를 이용하는 경우 측정값의 보정을 위해서 Bradford protein assay (Thermo Fisher Scientific)로 전체 단백질량 측정 후 차이 값을 보정해주었다.
6. Tyrosinase mRNA 발현량 측정
Tyrosinase mRNA의 발현을 확인하기 위해서 total RNA는 TRIzolTM (Invitrogen, Thermo Fisher Scientific)을 이용하여 추출하였다. 추출된 total RNA를 MaestroNano Pro Micro-Volume spectrophotometer (Maestrogen Inc., USA)를 이용하여 정량하고, 동일량을 Moloney Murine Leukemia Virus (M-MLV) reverse transcriptase (Invitrogen)로 cDNA를 합성하였다. 합성된 cDNA를 이용하여 tyrosinase의 발현량을 알아보는 quantitative real time polymerase chain reaction (qRT-PCR)은 StepOnePlusTM Real-Time PCR System (Applied Biosystems, Thermo Fisher Scientific)에서 진행하였다. PCR 반응액은 HOT FIREPol EvaGreen® qPCR Mix Plus (ROX) (Solis BioDyne, Estonia), 0.5 pmoles/μL forward primer, 0.5 pmoles/μL reverse primer, cDNA를 혼합하여 제조하였고, tyrosinase와 보정을 위해서 사용된 β-actin의 primer 정보는 Table 1과 같다. qRT-PCR 결과는 Ct값을 측정하여 2-ΔΔCT의 계산 방법을 이용하여 상대정량 하였고, 모든 값은 β-actin을 이용하여 샘플간의 차이를 보정하였다.
7. Tyrosinase protein 발현측정
Tyrosinase protein의 발현을 확인하기 위해서 western blot을 사용하여 발현을 분석하였다. 수확된 세포를 1% SDS lysis buffer (Promega, USA)로 95℃에서 20 min 용해시킨 후 5X sample buffer [10% SDS, 1M Tris-HCl (pH 6.8), 50% glycerol, 25% β-mercaptoethanol, 1% bromophenol blue] (Sigma-Aldrich)에 용해하고 Bradford protein assay kit로 전체 단백질량을 확인하여 동량의 단백질을 5X sample buffer에 섞어 12% sodium dodecyl sulfate polyacrylamide gel (SDS-PAGE) 전기영동하여 크기별로 분리하였다. 이 후 단백질을 polyvinylidene difluoride (PVDF) membrane (Millipore, USA)으로 옮겨 tyrosinase (M-19; Santa Cruz, USA)와 β-actin (Santa Cruz)를 각각의 target 단백질에 붙이고, secondary antibody를 추가로 붙여준 후 ClarityTM Western ECL Substrate (Bio-Rad, USA)를 도포하여 단백질이 발생되게 하고, 이를 Fusion FX7 imaging system (Vilber Lourmat, France)에서 촬영하여 단백질량을 확인하였으며 확인된 tyrosinase 단백질량은 β-actin을 이용하여 보정하였다.
8. MITF 전사활성 측정
MITF의 전사활성을 측정하기 위해서 MITF의 binding site가 들어있는 luciferase assay plasmid인 pGL3 (Invitrogen)를 사용하였다. Report plasmid인 pGL3-MITF와 normalization plasmid인 pCMV-β-gal을 Lipofectamine 2000 (Invitrogen)을 이용하여 형질 전환하였고, 24 hr의 안정화 시간을 거친 후 Cnidium officinale Makino 추출물로 처리하였다. 처리 후 수확된 세포는 ×1 luciferase lysis buffer (Promega, USA)를 이용하여 cell lysate를 얻고, luciferase 기질인 Luciferase Reporter 1000 Assay System (Promega)에 넣어주어 발광을 유도하고, 발광 정도는 Veritas™ Microplate Luminometer (Veritas, USA)로 측정하여 MITF의 전사활성을 확인하였다. 또한 O-nitrophenyl-β-D-galactopyranoside assays (β-Gal Assay Kit, Invitrogen)를 이용하여 실험에서 나올 수 있는 오차값을 보정하였다.
Results and Discussion
1. B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물의 세포독성
B16F10 mouse melanoma 세포에 Cnidium officinale Makino 추출물에 의한 세포독성을 확인하기 위해서, Cnidium officinale Makino 추출물을 0–200 μg/mL로 B16F10 mouse melanoma 세포에 24 h 처리 후 세포 생존율을 측정하였다. 200 μg/mL 농도까지 세포의 성장 억제가 일어나지 않는 것을 확인하였고, 이에 따라 Cnidium officinale Makino 추출물의 독성이 없는 농도로 확인된 200 μg/mL 이하에서 melanin 합성 저해실험을 진행하였다(Figure 1).
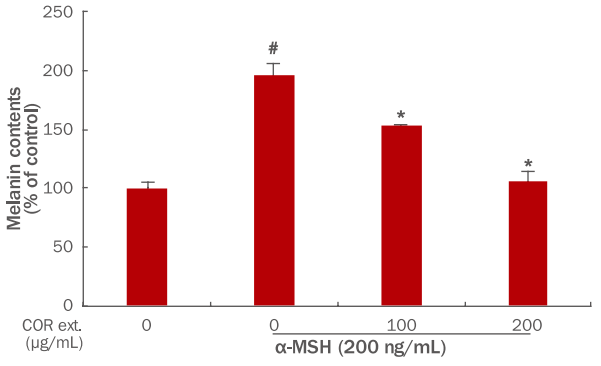
2. B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물에 의한 melanin 함량변화
Cnidium officinale Makino 추출물에 의한 melanin 함량변화를 확인하기 위해서 200 ng/mL α-MSH을 처리하고 동시에 Cnidium officinale Makino 추출물을 0, 100, 200 μg/mL 농도로 처리하였다. 48 h 배양한 후 세포를 파쇄하여 melanin 함량을 측정하였다. α-MSH 처리군에서는 melanin 함량이 196.24%까지 증가였고, Cnidium officinale Makino 추출물 100, 200 μg/mL로 처리시 다시 153.24%, 105.24%까지 감소하였다(Figure 2). Melanin 합성은 melanosome에서 tyrosinase에 의해서 생성되기 때문에 이후 실험에서 tyrosinase 활성을 측정하였다(Pillaiyar et al., 2017).
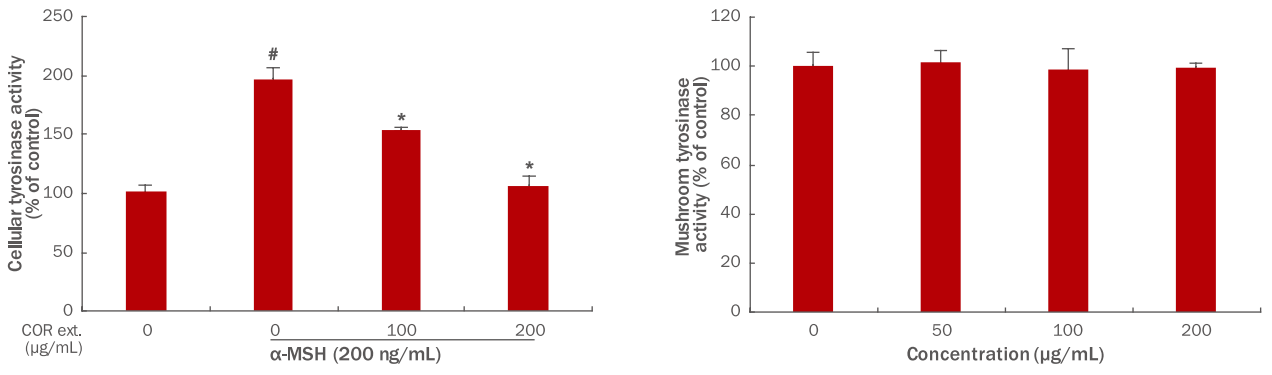
3. B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물에 의한 tyrosinase 활성 변화
Cnidium officinale Makino 추출물에 의한 melanin 생성감소가 tyrosinase에 의해서 일어나는지 확인하기 위해서 200 ng/mL α-MSH을 처리하고 동시에 Cnidium officinale Makino 추출물을 0, 100, 200 μg/mL 농도로 처리한 후 세포 내 tyrosinase 활성을 확인하였다. Figure 3A에서와 같이 세포 내 tyrosinase 활성이 농도의존적으로 감소됨을 확인하였다. 하지만 Cnidium officinale Makino 추출물이 mushroom tyrosinase에 의한 melanin 생성은 억제하지 못함을 확인하였다(Figure 3B). 때문에 Cnidium officinale Makino 추출물은 간접적으로 tyrosinase 발현 또는 활성 조절을 통해서 melanin합성을 저해함을 확인하였다.
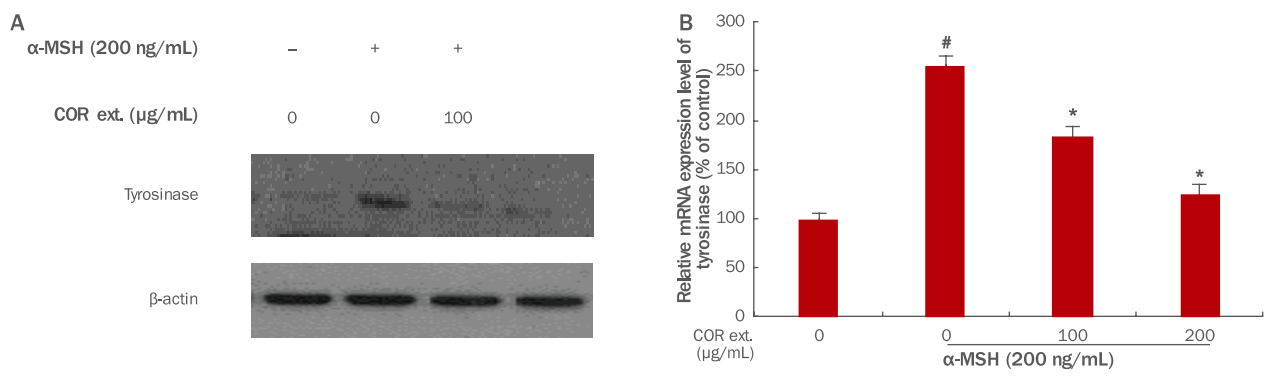
4. B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물에 의한 tyrosinase 발현변화
Cnidium officinale Makino 추출물에 의해 tyrosinase 발현이 조절되는지 알아보기 위해 mRNA와 단백질 발현량을 확인하였다. Tyrosinase의 단백질량을 확인결과 Cnidium officinale Makino 추출물에 의해서 발현이 의존적으로 감소됨을 확인하였다. 이러한 tyrosinase 발현 감소가 mRNA 억제에 의해서 일어나는지 확인하기 위해서 Cnidium officinale Makino 추출물을 처리하고 tyrosinase의 mRNA 발현량을 확인하였다. Figure 4B에서와 같이 tyrosinase mRNA는 Cnidium officinale Makino 추출물에 의해서 감소됨을 확인할 수 있었다.
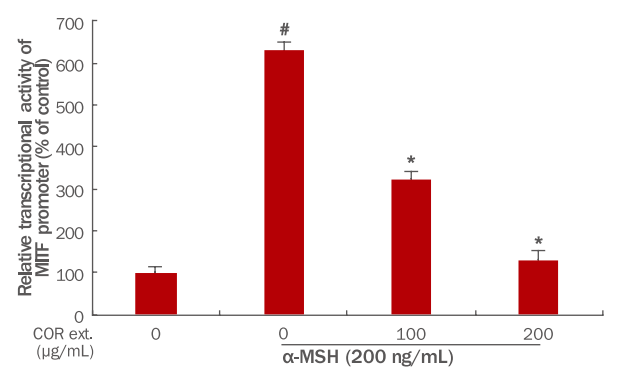
5. B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물에 의한 MITF 전사활성변화
α-MSH에 의한 melanin 합성에서 tyrosinase의 발현은 MITF에 의해서 발현이 조절된다(D'Mello et al., 2016; Hsiao & Fisher, 2014). 따라서 MITF의 전사활성이 Cnidium officinale Makino 추출물에 의해서 조절되는지 확인하였다. Figure 5에 보는 것과 같이 MITF의 전사활성은 α-MSH에서 증가되었다가, Cnidium officinale Makino 추출물에 의해서 감소함을 확인할 수 있었다. 때문에 Cnidium officinale Makino 추출물은 MITF의 전사활성을 감소시킴으로써 tyrosinase의 발현 및 활성을 억제하고, 이를 통해서 melanin합성이 저해됨을 확인할 수 있었다.
Conclusion
본 연구에서는 B16F10 mouse melanoma 세포주 실험모델 활용을 통해 Cnidium officinale Makino 추출물이 피부미백원료로서의 효능이 있음을 in vitro 에서 알아보고, 화장품 소재로서 Cnidium officinale Makino 추출물의 효용성을 확인하고자 하였다. 첫째, α-MSH가 처리된 B16F10 mouse melanoma 세포에서 Cnidium officinale Makino 추출물이 melanin 합성을 감소시킴을 확인하였다. 둘째, Cnidium officinale Makino 추출물이 melanin 합성에 가장 중요한 tyrosinase 발현 및 활성을 억제하는지 분석한 결과 α-MSH에 의해서 증가된 tyrosinase 발현 및 활성이 Cnidium officinale Makino 추출물에 의해서 감소함을 확인할 수 있었다. 또한 이러한 tyrosinase의 발현 감소는 MITF의 전사활성변화에 의해서 일어남을 확인할 수 있었다. 이러한 내용을 종합하여 보았을 때 Cnidium officinale Makino 추출물은 피부의 색소침착을 저해하는 미백 기능성 화장품 소재로서 가능성이 있을 것으로 판단된다.