This article has been corrected. See Asian J Beauty Cosmetol. 2023 Mar 30; 21(1): 175. 요약목적본 연구는 그릴루스 비마쿨루투스의 근감소증 억제 효과를 탐색하기 위해 일반성분과 아미노산, 지방산 조성과 함량을 분석하고, 근육세포(C2C12 cell line)에 그릴루스 비마쿨루투스 분말단백질과 알 추출물을 처리하였을때 근감소증 바이오마커인 마이오스타틴 발현에 미치는 영향을 확인하기 위하여 수행되었다.
방법그릴루스 비마쿨루투스 분말과 분말 단백질 추출물, 알, 알단백질 추출물 시료를 제조하여 아미노산은 자동분석기, 지방산은 gas chromatography 법으로 조성과 함량을 측정하였고, 일반성분은 AOAC 방법, 무기질 함량은 ICP-OES Ultima Expert를 사용하여 분석하였다. 근육세포에 그릴투스 비마쿨루투스 추출물을 농도별로 처리하여 세포활성을 측정한 후 마이오스타틴 발현 억제효과를 측정하였다.
AbstractPurposeCurrently, aging-related sarcopenia is considered a serious problem. However, few studies have addressed the treatment or prevention of sarcopenia using Gryllus bimaculatus. Therefore the present study was carried out to determine whether Gryllus bimaculatus has an ameliorative effect on sarcopenia and to study its applicability as a food for sarcopenia in the elderly or in patients with this condition.
MethodsThe contents of moisture, crude ash, crude protein, crude fat, carbohydrate and minerals were analyzed. The amino acid and fatty acid compositions were analyzed using an automatic amino acid analyzer and gas chromatography, respectively. Cell viability was measured using a 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide (MTT) assay. Myostatin expression was investigated in C2C12 cells using a luciferase reporter assay after treatment with a Gryllus bimaculatus extract.
ResultsThe Gryllus bimaculatus powder (GBP), protein extract of Gryllus bimaculatus (PEGB), Gryllus bimaculatus egg (GBE), and egg protein extract of Gryllus bimaculatus (EPGB) were high in essential amino acids, especially branched chain amino acids, and unsaturated fatty acids, and low in carbohydrates. Moreover, Gryllus bimaculatus appeared to have ameliorative effects on sarcopenia by suppressing the mRNA expression of myostatin in C2C12 cells.
中文摘要目的 目前,与衰老相关的肌肉减少症被认为是一个严重的问题。然而,很少有研究涉及使用 双斑蟋蟀治疗或 预防肌肉减少症。因此,本研究旨在确定双斑蟋蟀是否对肌肉减少症有改善作用,并研究其作为食物对老年人 或患有这种疾病的患者的肌肉减少症的适用性。方法:分析了水分、粗灰分、粗蛋白质、粗脂肪、碳水化合物 和矿物质的含量。分别使用自动氨基酸分析仪和气相色谱法分析氨基酸和脂肪酸组成。使用 3-(4,5-二甲基噻唑 -2-基)-2,5-二苯基溴化四唑 (MTT) 测定法测量细胞活力。在用双斑蟋蟀提取物处理后,使用荧光素酶报告基因 测定在 C2C12 细胞中研究肌生长抑制素表达。结果:双斑蟋蟀粉 (GBP)、双斑蟋蟀蛋白提取物 (PEGB)、双斑 蟋蟀卵(GBE)和双斑蟋蟀卵蛋白提取物(EPGB)富含必需氨基酸,尤其是支链氨基酸和不饱和脂肪酸,碳水化合物 含量低。此外,双斑蟋蟀似乎通过抑制C2C12细胞中肌肉生长抑制素的mRNA 表达来改善肌肉减少症。结论: 双斑蟋蟀将对食品材料的开发或预防老年人或患有这种疾病的患者的肌肉减少症产生积极影响。
Introduction전 세계적으로 급증하고 있는 노인인구는 건강상의 문제 뿐 아니라 사회적으로 과도한 의료비용 지출 등으로 국가적으로도 부담이 되고 있다. 우리나라도 2021년 기준 65세 이상의 인구가 8,537,023명으로 전국 고령 인구비율이 16.5%를 넘어서 전 세계에서 유래를 찾을 수 없을 정도로 빠르게 노인인구가 급증하고 있다(KOSIS, 2021). 노인의 건강상의 가장 큰 문제 중 하나는 근감소증이라 할 수 있다. 근감소증(sarcopenia)은 근육량과 근력 감소가 특징으로 노인, 대사증후군, 심혈관계 질환, 당뇨병, 신체장애로 인한 활동제한, 운동부족, 골다공증, 암환자, 스테로이드 같은 약제를 장기간 과다 사용, 비만, 다이어트 후, 면역력이 저하된 허약한 사람에게서 발생하는 만성 염증성 질환이다(Fanzani et al., 2012). 노인의 근육감소와 근력 저하는 잘 걷지 못하고 혼자서는 움직이지도 못하는 등 일상생활과 활동에 지장을 초래하고 각종 질환에의 노출 빈도를 높이고 골격계 질환을 유발해 노인의 건강을 위협하고 삶의 질을 저하시킨다(Rizzoli et al., 2013). 근감소증은 2017년 WHO에서 질병코드를 부여 받았으나 효과적인 치료 약은 아직 개발되지 않았으므로 예방이나 억제가 중요하다(Cho et al., 2019). 노인이나 환자의 근감소증을 억제하고 예방하는 방법에는 부작용 발생 위험이 없는 영양과 운동이 있으나 환자나 연령이 많은 노인은 운동을 하기도 어려운 경우가 많아 일상생활에서 쉽게 실천할 수 있는 영양요법이 중요하다(Liao et al., 2019). 근육을 형성하고 유지하기 위해서는 다양한 영양소가 필요하며 가장 중요한 것은 단백질로 알려져 있어 이에 대한 연구가 많이 진행되고 있다(Lonnie et al., 2018). 양질의 단백질 식품급원으로는 육류 등의 동물성 단백질 식품이 대표적이나 과잉섭취는 포화지방산과 콜레스테롤 등의 과다 섭취로 이어져 암, 당뇨병, 고혈압, 심혈관계 질환의 원인이 될 수 있다(Hegsted, 1993). 근육 증강이나 유지를 위해 일부에서 유청단백질을 섭취하는 경우도 많으나 이 또한 장기간의 과잉섭취는 각종 부작용을 유발할 수도 있으므로(Messina et al., 2018) 이를 대체할 단백질 급원에 대한 요구도는 그 어느때보다도 높으며 이에 적합한 식품소재로 세계적으로 오래전부터 식용해 온 곤충이 대두되었다. 곤충은 예로부터 전 세계에서 식용이나 약용으로 섭취되어 왔으며 조단백질 함량이 다른 단백질 급원식품에 비해 높아 대체 단백질 식품으로서 가치가 높으며 지방, 무기질 등의 영양소도 많이 함유되어 있어 영양적 가치가 매우 높다(van Huis et al., 2013). 식용되는 곤충은 포화지방이 많은 육류에 비해 포화지방과 탄수화물은 적고 단백질과 근육형성에 도움이 되는 분지아미노산(branched chain amino acid)과 무기질 함량이 많다(Han, 2020). 또한 다른 동물성 단백질 급원에 비해 적은 양의 사료를 필요로 하며 물소비량이 적고 온실가스와 암모니아 발생량이 낮아 자연친화적 식품소재이다(Lee et al., 2019). 그러나 아직까지 식용곤충에 대한 인식 부족으로 인한 거부감으로 인해 식용곤충의 활용은 미비하며 노인의 근감소 예방소재 개발이나 연구는 매우 미흡한 실정이다(No, 2010; Kim et al., 2020). 한편 근감소증 관련 연구에서 근육의 성장을 억제하는 것으로 알려진 마이오스타틴(myostatin, MSTN)은 주로 골격근에서 발현되는 것으로 알려져 있으며 마이오스타틴이 정상적으로 기능하지 않을 경우 근육량이 증가한다고 보고되어 있다(Rodriguez et al., 2014). 마이오스타틴은 골격근에서 발현되어 근육 성장 음성 조절자 역할을 하는 MuRF1 및 atrogin-1의 발현을 유도함으로써 근육 단백질(류신, 이소류신, 발린) 합성을 억제하여 근육 성장을 억제한다(Lee & McPherron, 2001). 이러한 마이오스타틴 억제를 통해 근성장을 유도하는 것이 근감소증 치료의 주된 표적으로 알려져 있다(Kang et al., 2021). 근육단백질의 구성성분인 분지아미노산인 류신, 이소류신, 발린은 그릴루스 비마클루투스에 많이 함유되어 있어(Kim et al., 2020) 근육 단백질 합성을 촉진시켜 마이오스타틴 발현을 억제할 수 있을 것으로 사료된다. 특히 최근에 노인인구가 급증하면서 근감소증에 대한 많은 연구가 진행되고 있으나 식용곤충 특히 그릴루스 비마쿨루투스를 이용한 근감소증 관련 연구는 거의 없다.
이에 본 연구에서는 식용곤충 그릴루스 비마쿨루투스(Gryllus bimaculatus)의 일반성분과 아미노산, 지방산 조성 및 함량을 분석하고 그릴루스 비마쿨루투스 추출물을 근육세포 (C2C12 cell line)에 처리하여 근육감소 관련 biomarker인 마이오스타틴 발현에 미치는 영향을 탐색하여 노화나 질환에 의한 근위축/근육감소 억제효과 가능성을 확인하고자 하였다.
Methods1. 연구재료본 실험에 사용한 그릴루스 비마쿨루투스는 귀뚜라미 농원(Chungbuk, Korea)에서 구입하여 2일간 절식시켜 세척한 다음 쪄서 건조(60℃)한 후 믹서기(DA 5000; Daesungartlon, Korea)로 분쇄 후 동결건조 한 다음 시료로 사용하였다.
2. 일반성분 분석그릴루스 비마쿨루투스 분말, 알의 일반성분은 공인분석화학자협회(Association of Official Analytical Chemists, AOAC) 방법(AOAC, 2005)에 따라 수분은 105℃ 상압가열건조법, 조단백질은 세미마이크로 킬달(semimicro kjeldahl)법, 조회분은 550℃ 직접회화법으로 분석하였다. 탄수화물 함량은 분석된 수분, 조단백질, 조지방, 조회분 함량으로부터 계산하였다.
3. 무기질 함량 분석쌍별귀뚜라미 분말, 알의 무기질 함량 분석은 ICP-OES Ultima Expert (HORIBA Jobin Yvon, France)를 사용하여 분석하였다. 분석방법은 시료 0.1 g에 질산 9 mL을 넣고 watch glass (직경 9 cm; ThermoFisher Scientific, USA)로 덮어 200℃에서 가열한 후 산에 의해 분해된 시료를 깨끗이 씻은 후 과염소산 용액(Wako, Japan) 3 mL을 넣고 다시 250℃에서 가열한 다음 washing 한 후 1% 질산(Wako)으로 15 g으로 맞춘 후 시료로 사용하였다.
4. 아미노산 조성 분석아미노산 분석을 위하여 그릴루스 비마쿨루투스 분말, 알과 분말, 알의 단백질 추출물에 6 N 염산용액(Wako) 30 mL을 둥근 플라스크에 넣고 혼합한 다음 130℃에서 24 h 동안 가수분해한 후 초순수로 희석시키고 여과지(0.45 μm; Whatman, UK)로 여과하였다. 가수분해 한 시료를 중화하여 3차 증류수로 희석한 후 고성능 액체 크로마토그래피(high performance liquid chromatography, HPLC; Ultimate3000 (pump, autosampler, oven and UV/Thermo dionex, USA) FL detector 1260FLD (Agilent, USA))를 이용하여 분석하였으며 분석조건은 다음과 같다. Inno C18 Column (4.6 mm×150 mm, 5 μm; YoungjinBiochrom, Korea)을 사용하였고 40 mM sodium phosphate, pH 7와 acetonitrile/methanol (Sigma-Aldrich, USA) (10:45:45 v/v%) 을 이동상으로 사용하였다. 이동상의 유속은 1.5 mL/min로 하였고 파장은 350 nm, 형광파장은 450 nm로 하였다.
5. 지방산 조성그릴루스 비마쿨루투스 분말, 알과 분말, 알 단백질 추출물의 지방산 조성은 Garcés & Mancha (1993)과 Lee et al. (2010)의 방법에 준하여 gas chromatography (Agilent 7890A; Aglient Technologies, USA)를 사용하여 분석하였다. Gas chromatography (GC) 조건은 Column은 DB-23 (60 mm×0.25 mm×0.25 μm; Agilent, USA), carrier 가스는 He, injection port 온도는 250℃이며, 검출기 온도는 280℃로 유지하였다.
6. 근육세포배양C2C12 근육세포는 American Type CultureCollection (ATCC; USA)에서 구매 하였고, 15% 우태혈청(fetal bovineserum, FBS; Gibco, USA), 2 mM L-glutamine, 1 mM pyruvate, penicillin (100 U/mL; Gibco), streptomycin (10 g/mL, Gibco)이 함유된 Dulbecco's Modified Eagle's Medium (DMEM; Sigma-Aldrich)에서 37℃, 5% CO2 조건하에서 배양하였다.
7. 세포독성평가그릴루스 비마쿨루투스 알과 단백질 추출물이 세포 독성에 미치는 영향은 MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide) assay 방법으로 측정하였다. 96 well plate에 C2C12세포를 3×105 cells/well 당 분주하여 배양한 후 그릴루스 비마쿨루투스 추출물(1.0 mg/mL, 0.1 mg/mL, 0.01 mg/mL)을 처리한 뒤 24시간 37℃에서 배양한 뒤 MTT 용액을 10 μL씩 가하고 37℃ CO2 incubator에서 2 h 동안 방치하고 상등액을 제거한 뒤 dimethyl sulfoxide (DMSO) 50 μL를 넣고 30 min간 실온에서 방치하여 formazan product를 용해시키고 ELISA platereader (Epoch; BioTek, Korea)를 사용하여 540 nm에서 흡광도를 측정하였다. 세포 생존율은 대조군 세포에 대한 백분율로 나타내었다.
8. 그릴루스 비마쿨루투스 첨가에 따른 근감소 관련 mRNA 발현 변화그릴루스 비마쿨루투스 알, 그릴루스 비마쿨루투스 분말 단백질 추출물이 근감소 관련 mRNA 발현에 미치는 영향은 myostatin 유전자를 primer로 사용한 qRT-PCR로 확인하였다. C2C12 골격근 세포를 4×105 cells/well로 37℃에서 12 h 동안 배양한 후 각각의 시료 10 μg/mL로 첨가하였다. 동일한 양의 DMSO를 대조군에 첨가하였다. Microplate Spectrophotometer (Epoch; BioTek)를 이용하여 total RNA를 추출하고 RNA의 양을 측정하였다. Cell scripts cDNA 합성 키트(Enzynomics, Korea)를 사용하여 2 μg의 mRNA를 cDNA로 전환시켰다. Myostatin-specific primer인 TOPrealTM qPCR 2X Pre-MIX (SYBR Green with high ROX; Enzynomics, Korea), cDNA 40 ng, forward 및 reverse primer 각각 10 pmole을 혼합한 후 Applied BiosystemsTM QuantStudioTM 3 Real-Time PCR system (ThermoFisher Scientific, USA) 이용하여 mRNA 발현을 측정하였다.
9. Luciferase reporter assaypGL4.15 vector에 MSTN promoter (-534-+132, 667 bp)를 XhoI과 BglII를 이용하여 삽입시켰다. 12 well에 5×104/well씩 세포를 seeding 한 후 15-16 시간 후에 PBS를 이용 세포 washing 후 Opti-MEM media 900 μL를 넣어주었다. Opti-MEM media 100 μL에 pGL4.15-MSTN promoter (1 μg, firefly luciferase Vector)와 pRL-TK (200 ng, Renilla luciferase)를 Lipofectamine 2000 (2 μL, Invitrogen)과 함께 동시에 섞어 준 후 세포에 100 μL씩 넣어 준 후 co-transfection 시켰다(이때 pGL4.15 공벡터는 negative control로 사용하였다). 4시간 후 media change 후 12 시간 후에 Dual-Luciferase® Reporter Assay System (Promega, USA)방법과 luminometer (EnSpire®Multimode Plate Reader, PerkinElmer, USA) 기기를 이용하여 luciferase activity (발광) 측정하였으며, pRL-TK는 loading control로 사용하였다.
Results and Discussion1. 그릴루스 비마쿨루투스 분말, 알의 일반성분과 함량그릴루스 비마쿨루투스 분말, 알의 일반성분은 Table 1에 제시하였다. 그릴루스 비마쿨루투스 분말의 수분은 3.45%, 회분 4.22%, 조단백질 59.43%, 조지방 19.75%, 탄수화물 13.15%, 알은 수분 15.86%, 회분 7.17%, 조단백질 48.21%, 조지방 2.18%, 탄수화물 26.76%이었다. 이는 Yoo et al. (2013)의 연구에서 갈색거저리의 조단백질 함량 50.32% 조지방 33.72%에 비해 조단백질 함량은 매우 많고 조지방 함량은 적게 함유되어 있었다. 그릴루스 비마쿨루투스알은 분말에 비해 수분 함량과 탄수화물 함량이 높았다. 그릴루스 비마쿨루투스 분말의 수분함량은 3.45%로 갈색거저리유충 2.90%보다는 다소 높고, 흰점박이꽃무지유충 6.66%보다는 낮고 장수풍뎅이 유충 1.63%보다는 높았다(Baek et al., 2017). 탄수화물 함량은 분말 13.15%로 갈색거저리유충 9.32% 보다는 높았고, 흰점박이꽃무지유충 10.56%와는 비슷하였으며 장수풍뎅이유충 28.61%보다는 낮았다(Baek et al., 2017). 조단백질 함량은 59.43%로 갈색거저리유충 50.32%, 흰점박이꽃무지유충 57.86%, 장수풍뎅이유충 39.31%보다 높아 식용곤충 중 가장 높았다(Baek et al., 2017). 조지방 함량은 19.75%로 흰점박이꽃무지유충 16.57% 보다는 약간 많았으나, 갈색거저리 유충 33.7%, 장수풍뎅이유충 25.21%보다는 낮았다(Baek et al., 2017). 지방함량보다 단백질 함량이 많은 것은 근육관련 질환이나 노인의 근감소 예방 및 중장년 이후 혈중 지질이 높아지는 것을 예방하기 위한 식품소재나 식품으로서도 긍정적이며, 특히 지방과 탄수화물 함량이 적어 다이어트 소재로서의 활용이 기대되는 뷰티 푸드 소재로도 활용될 수 있을 것으로 사료된다.
2. 그릴루스 비마쿨루투스 분말, 알의 무기질 성분과 함량그릴루스 비마글루투스 분말과 알의 무기질 성분은 Table 2에 제시한 바와 같다. 그릴루스 비마글루투스 분말의 무기질 성분은 칼슘 110.8 mg/100 g, 칼륨 724.7 mg/100 g, 나트륨 289.3 mg/100 g, 인 739.8 mg/100 g, 아연 22.1 mg/100 g이었으며, 그릴루스 비마글루투스 알에는 칼슘 446.5 mg/100 g, 칼륨 850.2 mg/100 g, 나트륨 234.9 mg/100 g, 인 1098.0 mg/100 g, 아연 7.4 mg/100 g이 함유되어 있었다. 본 연구에서 그릴루스 비마글루투스 분말의 칼슘함량은 110.8 mg/100 g으로 갈색거저리유충 34.9 mg/100 g에 비해 약 3배 가량 높았고, 장수풍뎅이 유충 302.4 mg/100 g보다는 낮게 나타났다. 알의 칼슘 446.5 mg/100 g은 분말보다 약 4배 많고 장수풍뎅이 유충보다도 많이 함유되어 있었다(Baek et al., 2017). 이는 식용되고 있는 돼지고기(3.39-6.12 mg/100 g)에 비해서는 월등하게 높았다(Baek et al., 2017). 그릴루스 비마클루수 분말의 칼륨 함량은 724.7 mg/100 g, 알은 850.2 mg/100 g으로 흰점박이꽃무지 유충 1,597 mg/100 g, 갈색거저리 유충 865.15 g/100 g보다 낮게 나타났다. 이상의 결과를 보면 그릴루스 비마글루투스 분말과 알에는 칼슘 함량이 매우 많이 함유되어 있어 노인과 환자의 근골격계 질환예방이나 개선(Han & Kim, 2019), 건강증진에도 긍정적일 것으로 사료된다. 또한 칼륨은 혈압을 낮추는 생리활성 기능이 있고 그릴루스 비마글루투스분말과 알은 칼륨에 비해 나트륨 함량은 낮아서(Ophir et al., 1983; Singer et al., 1990) 그릴루스 비마글루투스는 고혈압을 예방할 수 있는 기능성 소재로서의 활용도 기대할 수 있을 것이다.
3. 그릴루스 비마쿨루투스 분말, 알과 분말단백질, 알단백질 추출물의 필수아미노산 조성 성분과 함량그릴루스 비마쿨루투스 분말(GBP)과 분말 단백질 추출물(PEGB), 알(GBE)과 알 추출물(EPGB)의 필수아미노산 성분은 Table 3에 제시하였다. GBP에는 아르기닌 32189.42 mg/kg, 류신 25382.52 mg/kg, 발린 17186.31 mg/kg, 이소류신 12790.01 mg/kg, 트레오닌 12679.04 mg/kg, 페닐알라닌 12249.08 mg/kg, 리신 12050.90 mg/kg, 히스티딘 10380.00 mg/kg, 메티오닌 6077.52 mg/kg, 트립토판 340.03 mg/kg이 함유되어 있었으며, PEGB에는 아르기닌 2822.72 mg/kg, 류신 2753.34 mg/kg, 히스티딘 2763.08 mg/kg, 페닐알라닌 1367.50 mg/kg, 이소류신 1281.90 mg/kg, 발린 1147.28 mg/kg, 리신 900.17 mg/kg, 트레오닌 710.63 mg/kg, 메티오닌 679.55 mg/kg이 함유되어 있었다. GBE에는 류신 31366.70 mg/kg, 아르기닌 27971.04 mg/kg, 발린 22134.32 mg/kg, 이소류신 17635.62 mg/kg, 리신 17415.08 mg/kg, 페닐알라닌 17408.95 mg/kg, 트레오닌 13954.78 mg/kg, 히스티딘 9636.80 mg/kg, 메티오닌 7981.89 mg/kg, 트립토판 587.15 mg/kg이 함유되어 있었으며, EPGB에는 류신 33446.02 mg/kg, 아르기닌 26550.90 mg/kg, 히스티딘 11688.21 mg/kg, 페닐알라닌 21497.65 mg/kg, 이소류신 20484.18 mg/kg, 발린 20324.82 mg/kg, 메티오닌 10226.42 mg/kg, 리신 9877.64 mg/kg, 트레오닌 4252.78 mg/kg이 함유되어 있었다. 필수아미노산은 체내에서 합성되지 않아 반드시 식사로 섭취해야 하는 아미노산으로 그릴루스 비마쿨루투스 분말, 분말 단백질 추출물, 알, 알 단백질 추출물에는 10가지 필수아미노산이 골고루 다량 함유되어 있었다. 그릴루스 비마쿨루투스 분말과 분말 단백질 추출물, 알과 알 단백질 추출물 모두 분지아미노산(BCAA)인 류신, 이소류신, 발린을 많이 함유하고 있었는데 이러한 분지아미노산은 골격근에서 산화되어 근육의 에너지원으로 이용되며(Min et al., 2016), 근세포에서 단백질의 이화 작용을 억제시켜 근 세포의 단백질의 감소를 최소화 할 수 있고(Arsenault & Brown, 2017), 장기간 운동을 할 때에는 근육의 에너지원으로 사용되어 분지아미노산이 많이 함유된 그릴루스 비마쿨루투스는 근력증강(Na et al., 2016; No, 2010), 근육생성과정(Chong et al., 2017)에 관여해 노인과 환자들의 근감소 예방에 도움이 되는 기능성 식소재, 식품, 성장기 아동이나 청소년들 뿐 아니라 일반인들에게도 영양보충식 소재나 건강기능식품으로서의 활용가치가 있을 것으로 기대된다. 또한 과잉의 육류섭취로 인해 혈중 지질의 증가가 우려되는 사람들과 건강을 중요시 하는 현대인들의 요구에 부합되는 적합한 식량대체자원으로 식품소재나 각종 기능성 식품으로(Hwang & Choi, 2015; Kim et al., 2015), 운동선수를 위한 단백질 보충식품(Min et al., 2016), 환자를 위한 영양 보충식(Kang et al., 2017; Kim et al., 2015), 의약품과 기능성 화장품의 신소재 원료로도 개발될 가능성이 있을 것으로 사료된다. 리신도 많이 함유되어 있는데 리신은 콜라겐 합성에 관여하여 피부건강을 유지하고 피부노화를 억제하는데 도움을 주는 것으로 알려져 있어(Zhang et al., 2007) 향후 중노년 항피부노화소재로도 이용될 수 있을 것이다.
4. 그릴루스 비마쿨루투스 분말, 알과 분말단백질, 알단백질 추출물의 비필수아미노산 조성 성분과 함량그릴루스 비마쿨루투스 분말(GBP)과 분말 단백질 추출물(PEGB), 알(GBE)과 알 추출물(EPGB)의 성분은 Table 4에 제시하였다. GBP에는 비필수 아미노산인 글루탐산 36085.54 mg/kg, 알라닌 31947.01 mg/kg, 글리신 21944.58 mg/kg, 아스파르트산 19451.30 mg/kg, 세린 18447.13 mg/kg, 티로신 17053.70 mg/kg, 글루타민 6389.89 mg/kg, 타우린 3309.13 mg/kg, 프롤린 2834.81 mg/kg, GABA 104.353 mg/kg, PEGB에는 알라닌 1965.78 mg/kg, 글루탐산 3266.08 mg/kg, 글리신 2617.74 mg/kg, 아스파르트산 1571.11 mg/kg, 티로신 1351.96 mg/kg, 세린 730.02 mg/kg, 타우린 83.44 mg/kg이 함유되어 있었다. GBE에는 비필수 아미노산인 글루탐산 52610.30 mg/kg, 아스파르트산 46966.74 mg/kg, 세린 36770.57 mg/kg, 알라닌 20809.88 mg/kg, 티로신 18674.93 mg/kg, 글리신 10619.62 mg/kg, 프롤린 8147.20 mg/kg, 글루타민 1299.48 mg/kg, 타우린 161.38 mg/kg, EPGB에는 글루탐산 38892.00 mg/kg, 아스파르트산 24248.07 mg/kg, 티로신 22930.33 mg/kg, 글리신 12806.31 mg/kg, 알라닌 19435.89 mg/kg, 세린 6873.57 mg/kg, 프롤린 5229.67 mg/kg, GABA 104.353 mg/kg이 함유되어 있었다. 비필수 아미노산 중 프롤린은 리신과 함께 콜라겐 합성에 관여하므로(Zhang et al., 2007), 향후 중 노년 항노화 피부관련 소재로 활용될 수 있을 것이다(Na et al., 2016).
5. 그릴루스 비마쿨루투스 분말, 알과 분말단백질, 알단백질 추출물의 필수지방산 조성 성분과 함량그릴루스 비마쿨루투스 분말(GBP)과 분말 단백질 추출물(PEGB), 알(GBE)과 알 추출물(EPGB)의 필수지방산 조성 성분과 함량은 Table 5에 제시하였다. 오메가 6지방산인 리놀레산 함량은 EPGB 72.209 mg/g, GBP 60.411 mg/g, PEGB 53.474 mg/g, GBE 41.439 mg/g, 오메가 3지방산인 리놀렌산 함량은 EPGB 1.432 mg/g, GBP 1.170 mg/g, PEGB 0.908 mg/g, GBE 0.720 mg/g이었다. EPGB가 가장 많이 리놀렌산을 많이 함유하고 있었다.
6. 그릴루스 비마쿨루투스 분말, 알과 분말단백질, 알단백질의 비필수지방산 조성 성분과 함량그릴루스 비마쿨루투스 분말(GBP)과 분말 단백질 추출물(PEGB), 알(GBE)과 알 추출물(EPGB)의 비필수지방산 조성 성분과 함량은 Table 6에 제시하였다. 오메가 9 지방산인 올레산 함량은 EPGB 64.697 mg/g, GBP 60.570 mg/g, GBE 56.509 mg/g, PEGB 40.822 mg/g, EPGB 34.943 mg/g, 그외 팔미트산 함량은 GBE 59.154 mg/g, GBP 52.162 mg/g, PEGB 16.243 mg/g, 스테아르산 함량은 GBP 15.159 mg/g, GBE 13.566 mg/g, EPGB 7.835 mg/g, PEGB 4.818 mg/g이었다. 그릴루스 비마쿨루투스 분말(GBP)과 분말 단백질 추출물(PEGB), 알(GBE)과 알 추출물(EPGB) 모두 올레산이 가장 많이 함유되어 있었다. 이는 동물성 식품에 비해 불포화지방산 함량이 월등히 높다(Ha et al., 2014). 특히 올레산이 가장 많이 함유되어 있는데 이는 Singer et al. (1990)에 따르면 올레산과 리놀레산은 혈중 LDL 콜레스테롤을 낮추고 혈압을 낮추어 주는 효능이 우수하다고 알려져 있어 이를 이용한 식품이나 식소재는 혈행개선에 도움을 줄 수 있을 것으로 사료된다. 또한 기능성식품이나 신약소재로도 활용될 수 있을 것으로 기대되는 바이다.
7. 그릴루스 비마쿨루투스 추출물의 근육세포에 대한 세포독성 평가그릴루스 비마쿨루투스 추출물의 근육세포(C2C12)에 대한 세포 활성도는 MTT assay 방법을 수행하여 측정하였다. MTT assay는 tetraaolium salt가 미토콘드리아에서 생성되는 NADH, NADPH에 의해서 환원되어 생성되는 formazan을 540 nm 흡광도로 측정하여 세포의 생존율을 확인하는 방법이다(Vajrabhaya & Korsuwannawong, 2018). GBE와 PEGB를 각각 0.01, 0.1, 1.0 mg/mL의 농도로 처리하여 control 군과 비교하였을 때, GBE 87.5%, 68.75%, 50.0%, PEGB 76.4%, 64.7%, 47.5%의 세포생존율을 나타내어 2 군 모두 0.01 mg/mL에서 독성을 나타내지 않았다(Figure 1). 이 결과를 바탕으로 마이오스타틴 발현에 미치는 영향에 대한 확인은 0.01 mg/mL의 농도를 설정하여 진행하였다.
8. 근육세포에서 그릴루스 비마쿨루투스 추출물과 단백질 추출물이 마이오스타틴 발현에 미치는 영향근육세포에 GBE와 PEGB가 세포내 근육세포 생성에 영향을 미쳤는지 확인하기 위하여 근육성장 억제에 관여하는 전사인자 마이오스타틴(myostin, MSTN)의 mRNA 발현을 확인한 결과 GBE와 PEGB 각각 0.01 mg/mL로 12 h, 24 h 처리하였을 때 24 h 후에 대조군에 비해 약 44%와 72% 정도 감소하였다(Figure 2). Myostin promoter luciferase vector를 이용한 활성은 GBP와 PEGB에 의해 35.9%, 13.6% 정도 억제되었다(Figure 3). 마이오스타틴은 골격근 성장을 음성 피드백으로 조절하는 전사인자로 근세포의 성장과 발달을 저해하는 것으로 알려져 있는 바이오 마커이므로 이의 발현을 억제하는 것은 근감소증을 억제하는 효과가 있는 것으로 알려져 있다(Amthor, 2004; Fakhfakh et al., 2011). 본 실험결과에서 그릴루스 비마쿨루투스 추출물이 마이오스타틴 발현을 억제한 것은 근감소증 억제 효과 가능성이 있는 것으로 사료된다. 즉, GBE와 PEGB는 마이오스타틴의 프로모터 활성 억제를 통한 마이오스타틴의 mRNA 발현을 억제하여 근감소증 억제 효능이 있으며, GBE에 비해 PEGB가 효과적일 것으로 보이나 이에 대한 연구는 더 진행되어야 할 것으로 사료된다.
Conclusion이상의 결과 그릴루스 비마쿨루투스 분말과 분말 단백질 추출물, 알, 알단백질 추출물 모두 단백질 함량이 많고 탄수화물 함량은 적게 함유되어 있었다. 특히 필수아미노산 조성이 우수하였고 분지아미노산인(류신, 이소류신, 발린) 함량이 많았다. 지방산조성은 올레산이 많이 함유되어 있었다. 무기질은 칼슘과 칼륨이 많이 함유되어 있었다. 그릴루스 비마쿨루투스는 마이오스타틴 프로모터 활성 억제를 통한 마이오스타틴 mRNA 발현을 억제하였다. 즉, 그릴루스 비마쿨루투스는 분지아미노산이 많이 함유되어 있고 근육세포에서 마이오스타틴 발현을 억제하여 노약자와 근육질환 환자를 위한 근감소 억제 기능성 소재나 식품으로 활용하거나 개발할 가능성이 있는 것으로 사료된다. 향후 그릴루스 비마쿨루투스을 이용한 근감소 억제 기전과 이를 활용한 식품에 관한 다양한 연구가 이루어지길 기대하는 바이다.
AcknowledgementsThis work was supported by grants from Basic Science Research Program through the National Research Foundation of Korea (NRF) funded by the Ministry of Education (NRF-2019R1I1A1A01041076).
NOTESAuthor's contribution
JSH designed, interpreted data, and wrote the manuscript. SHK performed experiment of research project and SMK helped to wrote the manuscript. Korea Basic Science Institute supported experiment equipment. All tables and figures are created by the author's.
Author details
Si-Hyun Kim (Researcher), Neuroscience Research Center, Department of Pharmacology, College of Medicine, Seoul National University, 103 Daehakro, Jongro-gu, Seoul 03080, Korea; Su-Min Ko (Undergraduate Research Student), Department of Chem ica l and Biological Engineering, Korea University, School of Civil, Environmental and Architectural Engineering, College of Engineering, Korea University, 145 Anam-ro, Seongbuk-gu, Seoul 02841, Korea; Jung-Soon Han (Instructor), Korea University Graduate School of Human Ecology, 145 Anam-ro, Seongbuk-gu, Seoul 02841, Korea.
Figure 1.Viability of C2C12 cells treated with GBE and PEGB.The different letters included in the bar graphs for each test indicate significant differences, as determined using Duncan’s multiple range test (**p<0.01, ***p<0.001). GBE and PEGB at a concentration of 0.01 mg/mL failed to decrease cell viability.
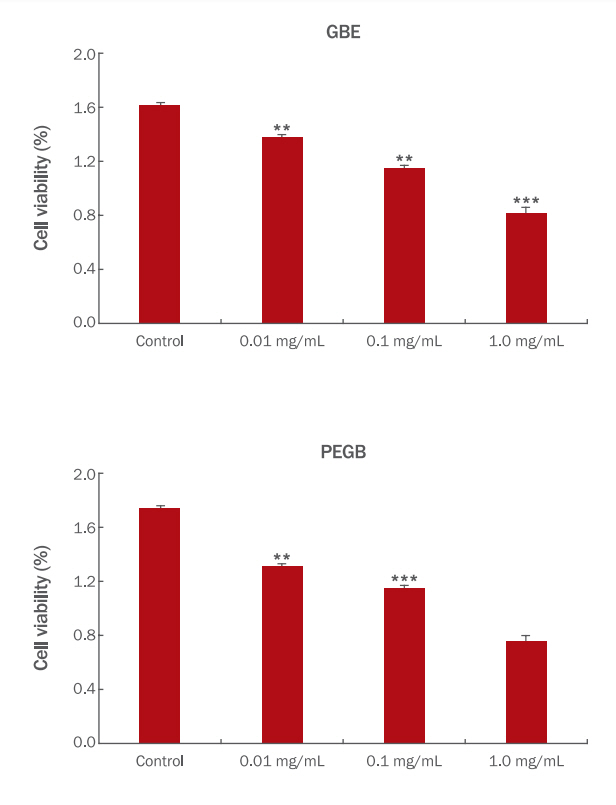
Figure 2.Relative mRNA expression levels of myostatin in C2C12 cells treated with GBE and PEGB at 0.01 mg/mLThe different letters included in the bar graphs for each test indicate significant differences, as determined using Duncan’s multiple range test (*p<0.05, **p<0.01, ***p<0.001). GBE and PEGB induced a decrease in the expression of myostatin at 24 h after the on set of treatment.

Figure 3.Relative myostatin (MSTN) promoter activity in C2C12 cells treated with GBE and PEGB, as assessed using a luciferase assay.The different letters included in the bar graphs for each test indicate significant differences, as determined using Duncan’s multiple range test (*p<0.05). GBP and PEGB induced a decrease in the expression of myostatin.
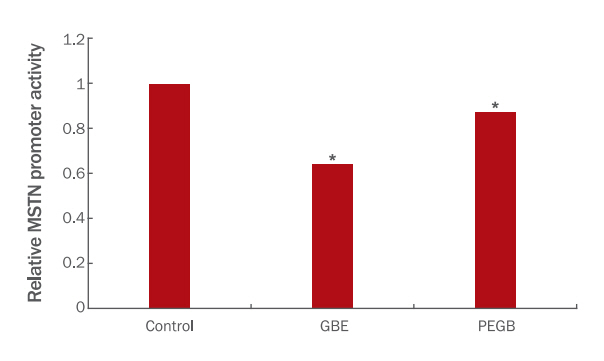
Table 1.General composition of the powder, and egg of Gryllus bimaculatus (Unit: %)
Table 2.Mineral content of the powder, and egg of Gryllus bimaculatus (Unit: mg/100g)
Table 3.Essential amino acid content of Gryllus bimaculatus powder, egg, powder protein extract, and egg protein extract (Unit: mg/kg) Table 4.Nonessential amino acid content of Gryllus bimaculatus powder, egg, powder protein extract, and egg protein extract (Unit: mg/kg) Table 5.Essential fatty acid content of Gryllus bimaculatus powder, egg, powder protein extract, and egg protein extract (Unit: mg/g)
Table 6.Nonessential fatty acid content of Gryllus bimaculatus powder, egg, powder protein extract, and egg protein extract (Unit: mg/g) ReferencesAOAC. Official methods of analysis. 18th ed. Association of Officiating Analytical Chemists. Washington DC. pp112-113. 2005.
Amthor H, Nicholas G, McKinnell I, Kemp CF, Sharma M, Kambadur R, Patel K. Follistatin complexes myostatin and antagonizes Myostatin-mediated inhibition of myogenesis. Developmental Biology 270: 19-30. 2004.
Arsenault JE, Brown KH. Effects of protein or amino-acid supplementation on the physical growth of young children in low-income countries. Nutrition Reviews 75: 699-717. 2017.
Baek M, Hwang JS, Kim MA, Kim SH, Goo TW, Yun EY. Comparative analysis of nutritional components of edible insects registered as novel foods. Journal of Life Science 27: 334-338. 2017.
Cho HT, Sim KS, Kim Y, Chang MH, Kim T, Lee SH, Lee DH, Kim JH. Anti-diabetic activity of edible insect Gryllus bimaculatus extracts in insulin-deficient diabetic mice. Journal of the Korean Society of Food Science and Nutrition 48: 1165-1171. 2019.
Chong HS, Kim SY, Cho SR, Park HI, Baek JE, Kuk JS, Suh HJ. Characteristics of quality and antioxidant activation of the cookies adding with mealworm (Tenebrio molitor) and black bean powder. Journal of Food Hygiene and Safety 32: 521-530. 2017.
Fanzani A, Conraads VM, Penna F, Martinet W. Molecular and cellular mechanisms of skeletal muscle atrophy: an update. Journal of Cachexia, Sarcopenia and Muscle 3: 163-179. 2012.
Fakhfakh R, Michaud A, Tremblay JP. Blocking the myostatin signal with a dominant negative receptor improves the success of human myoblast transplantation in dystrophic mice. Molecular Therapy 19: 204-210. 2011.
Garcés R, Mancha M. One-step lipid extraction and fatty acid methyl esters preparation from fresh plant tissues. Analytical Biochemistry 211: 139-143. 1993.
Ha JJ, Kim BK, Yi JK, Oh DY, Kim SS, Kim TK, Chae HB, Kim SJ, Park YS. Cortisol and fatty acid contents in Hanwoo meat produced by antibiotics-free rearing system. Reproductive and Developmental Biology 38: 129-136. 2014.
Han JS. Improving awareness on edible insects through dietary education based on health belief model. Asian Journal of Beauty and Cosmetology 18: 549-558. 2020.
Hegsted DM, Ausman LM, Johnson JA, Dallal GE. Dietary fat and serum lipids: an evaluation of the experimental data. The American Journal of Clinical Nutrition 57: 875-883. 1993.
Hwang SY, Choi SK. Quality characteristics of muffins containing mealworm (Tenebrio molitor). Culinary Science & Hospitality Research 21: 104-115. 2015.
Kang MJ, Moon JW, Lee JO, Kim JH, Jung EJ, Kim SJ, Oh JY, Wu SW, Lee PR, Park SH, Kim HS. Metformin induces muscle atrophy by transcriptional regulation of myostatin via HDAC6 and FoxO3a. Journal of Cachexia, Sarcopenia and Muscle 13: 605-620. 2021.
Kang MS, Kim MJ, Han JS, Kim AJ. Fatty acid composition and anti-inflammatory effects of the freeze dried Tenebrio molitor Larva. The Korean Journal of Food and Nutrition 30: 251-256. 2017.
Kim HM, Kim JN, Kim JS, Jeong MY, Yun EY, Hwang JS, Kim AJ. Quality characteristics of patty prepared with mealworm powder. The Korean Journal of Food and Nutrition 28: 813-820. 2015.
Kim YJ, Kim YK, Han JS. Perception of edible insect and insect foods among adults. Asian Journal of Beauty and Cosmetology 18: 53-63. 2020.
KOSIS (Statistics Korea, 2021 Older statistics), 2021.09.29.
Lee BY, O JH, Kim MH, Jang KH, Lee JC, Surh JH. Influences of roasted or non-roasted brown rice addition on the nutritional and sensory properties and oxidative stability of Misutkaru, Korean heated cereal powder. Korean Journal of Food and Cookery Science 26: 872-886. 2010.
Lee SJ, McPherron AC. Regulation of myostatin activity and muscle growth. Proceedings of the National Academy of Sciences of the United States of America 98: 9306-9311. 2001.
Lee SM, Han JS, Kim AJ. Quality evaluation of Perilla seed gangjung added with mealworm powder. Asian Journal of Beauty and Cosmetology 17: 187-197. 2019.
Liao Y, Peng Z, Chen L, Zhang Y, Cheng Q, Nüssler AK, Bao W, Liu L, Yang W. Prospective views for whey protein and/or resistance training against age-related Sarcopenia. Aging and Disease 10: 157-173. 2019.
Lonnie M, Hooker E, Brunstrom JM, Corfe BM, Green MA, Watson AW, Williams EA, Stevenson EJ, Penson S, Johnstone AM. Protein for life: review of optimal protein intake, sustainable dietary sources and the effect on appetite in ageing adults. Nutrients 10: 360. 2018.
Messina M, Lynch H, Dickinson JM, Reed KE. No difference between the effects of supplementing with soy protein versus animal protein on gains in muscle mass and strength in response to resistance exercise. International Journal of Sport Nutrition and Exercise Metabolism 28: 674-685. 2018.
Min KT, Kang MS, Kim MJ, Lee SH, Han JS, Kim AJ. Manufacture and quality evaluation of cookies prepared with mealworm (Tenebrio molitor) powder. The Korean Journal of Food and Nutrition 29: 12-18. 2016.
Na EJ, Jang HH, Kim GR. Review of recent studies and research analysis for anti-oxidant and anti-aging materials. Asian Journal of Beauty and Cosmetology 14: 481-491. 2016.
No JK. A study of the sarcopenic obesity in aging. Asian Journal of Beauty and Cosmetology 8: 139-148. 2010.
Ophir O, Peer G, Gilad J, Blum M, Aviram A. Low blood pressure in vegetarians: the possible role of potassium. The American Journal of Clinical Nutrition 37: 755-762. 1983.
Rizzoli R, Reginster JY, Arnal JF, Bautmans I, Beaudart C, Bischoff-Ferrari H, Biver E, Boonen S, Brandi ML, Chines A, et al. Quality of life in sarcopenia and frailty. Calcified Tissue International 93: 101-120. 2013.
Rodriguez J, Vernus B, Chelh I, Cassar-Malek I, Gabillard JC, Hadj Sassi A, Seiliez I, Picard B, Bonnieu A. Myostatin and the skeletal muscle atrophy and hypertrophy signaling pathways. Cellular Molecular Life Sciences 71: 4361-4371. 2014.
Singer P, Jaeger W, Berger I, Berleben H, Wirth M, Richter-Heinrich E, Voigt S, Gödicke W. Effects of dietary oleic, linoleic and alpha-linolenic acids on blood pressure, serum lipids, lipoproteins and the formation of eicosanoid precursors in patients with mild essential hypertensio. Journal of Human Hypertension 4: 227-233. 1990.
Vajrabhaya L, Korsuwannawong S. Cytotoxicity evaluation of a Thai herb using tetrazolium (MTT) and sulforhodamine B (SRB) assays. Journal of Analytical Science and Technology 15-20. 2018.
van Huis A, Van ltterbeeck J, Klunder H, Mertens E, Halloran A, Muir G, Vantomme P. FAO. Edible insects: future prospects for food and feed security. Food and Agriculture Organization of the United Nations. Rome. pp45-105. 2013.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||