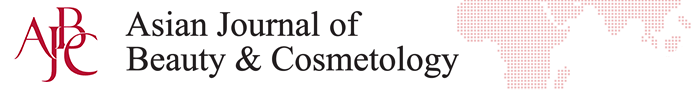황기 에탄올 추출물 및 생물전환 추출물의 항산화, 미백, 항염증 효과에 대한 생리활성
요약
목적
황기 에탄올 추출물과 생물전환 추출물의 기능성 화장품 소재로서의 활용 가능성을 확인하고자 하였다.
방법
항산화 및 미백, 항염증 효능을 확인하기 위하여 황기 에탄올 추출물과 생물전환 추출물의 2,2-diphenyl-1-picrylhydrazyl (DPPH) 라디칼 소거능, 멜라닌 생성 억제능, melanogenesis associated transcription factor (MITF)와 tyrosinase 발현량, nitric oxide (NO) 생성 억제능, cyclooxygenase 2 (COX2) 발현 억제 효과를 측정하였다.
결과
황기 에탄올 추출물과 생물전환 추출물의 두 시료 모두 0.5% 농도에서 51% 이상의 DPPH 라디칼 소거 활성을 확인하였다. 두 추출방법 모두 뛰어난 멜라닌 생합성 억제 효과를 확인하였으며, 생물전환 추출물의 MITF 발현 억제 효과를 확인하였다. 또한 생물전환 추출물은 우수한 NO 생성 억제 효과를 확인하였으나, COX2 억제 효과는 미비한 것으로 확인하였다.
결론
항산화 활성 효과를 가지는 생물전환 추출물이 MITF 활성 억제를 통한 미백 개선 및 NO 생성 억제를 통한 항염증 효과를 가지는 다양한 기능성 화장품 소재로서의 활용 가치가 있을 것으로 사료된다.
핵심용어: 항산화, 항염증, 황기, 생물전환, 멜라닌
Abstract
Purpose
This study aimed to analyze the applicability of Astragalus membranaceus ethanol extracts (AM) and Astragalus membranaceus bioconversion extracts (AMB) as an ingredient in functional cosmetics.
Methods
2,2-Diphenyl-1-picrylhydrazyl (DPPH) radical elimination, melanogenesis inhibition, melanogenesis associated transcription factor (MITF), and tyrosinase expression were evaluated. Furthermore, nitric oxide (NO) synthesis inhibition and its inhibitory effects on the expression of cyclooxygenase 2 (COX2) were evaluated.
Results
There were DPPH radical scavenging activities over 51% in 0.5% concentration of both samples. Both extraction methods had excellent melanin biosynthesis inhibition effects, and inhibitory effects on MITF expression were confirmed in the AMB. In addition, in the AMB, excellent inhibitory effects on NO production were confirmed, but COX2 inhibition effects were not great.
Conclusion
The AMB, which has anti-oxidant activity effects, is expected to be used as material for various functional cosmetic products that have whitening effects through MITF expression inhibition and anti-inflammatory effects through NO production inhibition.
Keywords: Anti-oxidant effects, Anti-inflammatory effects, Astragalus membranaceus, Bioconversion, Melanin
中文摘要
目的
探讨黄芪乙醇提取物和生物转换提取物作为功能性化妆品原料的活用可行性。
方法
为确认黄芪乙醇提取物和生物 转换提取物的抗氧化、美白以及抗炎功效,测定2,2-diphenyl-1-picrylhydrazyl(DPPH)自由基消除能力、黑色素生成抑 制能力、melanogenesis associated transcription factor(MITF)和酪氨酸酶表达程度、一氧化氮(nitric oxide,NO)抑 制作用以及cyclooxygenase 2(COX2)表达的抑制作用。
结果
黄芪乙醇提取物和生物转换提取物在0.5%浓度下,都具 有51%以上的DPPH自由基消除能力。两种提取物都具有良好的黑色素生成抑制作用,并确认了生物转换提取物对MITF 表达具有抑制作用。此外,生物转换提取物具有优秀的NO生成抑制作用,但抑制COX2作用并不显著。
结论
黄芪生物转 换提取物具有抗氧化作用,通过抑制MITF活性改善美白效果以及通过抑制NO生成具有抗炎作用,因此作为多种作用的化 妆品原料充分具有活用价值。
关键词: 抗氧化, 抗炎, 黄芪, 生物转换, 黑色素
Introduction
황기(黃芪, Astragali Radix)는 콩과(Leguminosae)에 속하는 다년생 초본 식물이며, 학명은 Astragalus membranaceus Bunge로 한방에서는 매우 중요한 한약재 중의 하나로 알려져 있다( Lee et al ., 2008). 국내에서는 강원도, 경상북도의 고산에 주로 분포되어 있으며, 국내에서 주로 발견되는 제주황기( Astragalus membranaceus var. alpinus Nakai), 개황기( Astragalus uliginosus L), 자주황기[ Astragalus dahuricus(Pall.) DC.], 정선황기( Astragalus koraiensis Y.N.Lee), 그 외 염주황기( Astragalus membranaceus var. mandshuricus Nakai), 설령황기( Astragalus setsureianus Nakai), 자주개황기( Astragalus adsurgens), 갯황기( Astragalus sikokianus Nakai), 긴꽃대황기( Astragalus schelichovii Turcz.) 등이 알려져 있고, 특히 편경(扁莖)황기[ Astragalus complanatus R. Brown (Leguminosae)]는 주로 약용으로 이용되고 있다( Bang et al., 2004). 황기의 주요 생리활성 성분으로는 미량광물질(trace elements), 사포닌(saponins), 아미노산(amino acids), 다당류(polysaccharides), 플라보노이드(flavonoids) 등이 보고되었으며( Ma et al., 2002), 황기의 뿌리에는 감마아미노뷰티르산(γ-aminobutyric acid, GABA)과 알파아미노부티르산(α-aminobutyric acid), 아스파라긴(asparagine), 베타인(betaine), 베타시토스테롤(β-sitosterols), 글루콘산(gluconic acid), 리놀레산(linoleic acid) 등의 여러 생리활성물질이 함유되어 있다고 알려져 있다( McKenna et al., 2002). 황기와 관련한 선행 연구로는 항산화 활성 연구( Kang et al., 2006; Kim & Yang, 2001), 혈관 형성 촉진 효과( Seo et al., 2007), 항염증 효과( Ryu et al., 2008), 동물 모델에서의 외과적 창상에 대한 치료 효과( Han et al ., 2005), 보습 및 항노화 효과( Jung et al., 2006; Kim et al., 2007) 등이 보고 되고 있다. 최근 천연 소재를 활용한 기능성 화장품의 소재 개발 연구가 진행되고 있으며( Ha & You, 2016; Han et al ., 2016; Yu & Kim, 2017), 천연 소재 개발과 더불어 소재에 대한 다양한 방법을 활용한 추출법을 적용하여 생물학적 활용성을 높이기 위한 연구가 활발하게 진행되고 있다. 특히 다양한 추출법 중 주목받고 있는 방법이 발효와 효소사용을 통해 유효한 성분의 함량을 높이는 생물전환 방법으로서, 생물전환은 생물학적 활성이 뛰어난 특정 유효성분들의 함량을 높여서 효능을 증가시키고 유효성분이 피부에 빠르게 흡수될 수 있도록 하는데 목적을 두고 있으며, 현재까지 생물전환을 통한 긍정적인 연구 사례가 보고 되고 있는 실정이다. 따라서 본 연구에서는 70% 에탄올로 추출한 황기 추출물과 효소처리를 이용하여 생물전환된 황기 추출물을 이용하여 항산화 활성을 확인하고, neutral red (NR) assay를 이용한 B16F10 세포와 RAW 264.7 세포에서의 세포 생존율을 확인하였다. 미백 효과를 확인하고자 B16F10 세포에서의 멜라닌 생성 억제 효과와 MITF, tyrosinase 활성억제 효과를 측정하였고, NO 생성 억제 및 COX2 활성 억제를 통한 항염증 효과를 평가함으로써 70% 에탄올 추출법과 생물전환 추출법을 활용한 황기 추출물이 기능성 화장품 소재로서의 활용 가능성을 확인하고자 하였다.
Methods
1. 실험재료
1) 에탄올 추출
건조된 황기는 제천한방약초(Korea)에서 구입하였으며, 70% 에탄올(Duksan Pure Chemicals, Korea)은 황기 시료 무게의 10배를 가하여 37℃, 100 rpm 인큐베이터(Jeio Tech, Korea) 안에서 72 h 동안 추출하였다. 얻어진 추출물의 상층액을 정제하고, 추출용매인 에탄올을 감압 농축(Eyela, Tokyo Rikakikai, Japan)을 통해 제거한 뒤 동결 건조(ilShinBioBase, Korea)하여 황기 에탄올 추출물(Astragalus membranaceus ethanol extracts, AM)을 제조하였다. 건조중량에 대한 추출 고형분의 수율은 12.33%로 확인되었다.
2) 생물전환
위와 같이 획득한 황기 에탄올 추출물에 복합 효소(AccelleraseⓇ 1500; DuPont, USA)를 처리하여 효소에 의한 가수분해 후, 50℃ high temperature drying oven (Changshin Science, Korea)에서 진공 건조하여 50% oxyresveratrol을 포함하는 황기 생물전환 추출물(Astragalus membranaceus bioconversion extracts, AMB)을 제조하였다.
3) 세포주 및 세포배양
본 실험에 사용한 세포주인 B16F10 melanoma, RAW 264.7 macrophage 세포는 한국세포주은행(Korean Cell Line Bank, Korea)에서 구입하여 사용하였으며, high glucose Dulbecco’s modified Eagle’s medium (high glucose DMEM; Sigma-Aldrich, USA) 배지에 10% fetal bovine serum (FBS; Sigma-Aldrich)과 1% penicillin/streptomycin (100 IU/mL, 50 μg/mL; Sigma-Aldrich)를 첨가하여 37℃, 5%의 CO2 습윤 배양기(Jeio Tech)에서 배양하였다.
2. 항산화 효과 측정
AM과 AMB의 항산화 효과를 확인하기 위해 Blois (1958) 방법을 이용하여 DPPH 라디칼 소거능을 측정하였다. 각 시료의 최종농도가 0.05, 0.1, 0.25, 0.5%가 되도록 에탄올에 희석한 후 10 mM DPPH (Sigma-Aldrich) 용액 180 μL와 시료액 20 μL를 96 well plate에 분주하여 37℃에서 30 min 동안 반응시킨 다음 microplate reader (Synergy HT, BioTek Instruments, USA)를 이용하여 517 nm에서 흡광도를 측정하였다. 양성 대조군으로는 0.01, 0.1, 1% 농도의 ascorbic acid (Sigma-Aldrich)를 사용하였다.
3. NR assay를 이용한 세포 생존율 측정
AM과 AMB가 세포 생존율에 미치는 영향을 확인하기 위하여 NR assay를 이용하여 측정하였다. B16F10 세포와 RAW 264.7 세포를 96 well plate에 3×104 cells/well의 농도로 분주하여 24 h 배양 후 AM과 AMB를 3.12, 6.25, 12.5, 25, 50 μg/mL의 농도로 희석하여 각 well plate에 처리하여 48 h 동안 배양하였다. 48 h 후 무 혈청 배지에 1% NR solution (Sigma-Aldrich) 용액이 첨가된 배양액으로 교환하여, 3 h 동안 배양한 후 phosphate buffered saline (PBS; Sigma-Aldrich)에 10% formaldehyde (Sigma-Aldrich) 용액을 첨가하여 각 well에 100 μL씩 분주하여 20 min 동안 고정하였다. NR desorb solution [1% glacial acetic acid (Sigma-Aldrich), 49% ethanol (Duksan Pure Chemicals), 50% distilled water]을 각 well에 100 μL씩 분주하여 세포 내의 NR을 추출한 다음 microplate reader를 이용하여 540 nm에서 흡광도를 측정하였다. 본 실험의 세포 생존율은 다음의 식에 따라 산출하였다.
4. 멜라닌 생합성 억제능 측정
AM과 AMB의 멜라닌 생합성 억제능은 B16F10 melanoma 세포를 이용하여 측정하였다( Lim et al ., 2003). B16F10 세포를 96 well plate에 각 well 당 2×10 3 cells/well의 농도로 분주하고 24 h 동안 배양하였다. 배양 후 멜라닌 생성을 촉진하기 위하여 5% FBS와 100 nM α-melanocyte-stimulating hormone (α-MSH; Sigma-Aldrich)가 포함된 배지로 교체하였고, 각 시료를 3.12, 6.25, 12.5, 25 μg/mL의 농도로 처리하여 72 h 배양하였다. 멜라닌 생성량은 microplate reader를 이용하여 405 nm에서 흡광도를 측정하였고, 멜라닌 생성억제량은 100 nM α-MSH로 처리한 대조군과 비교하여 백분율로 표시하였다. 양성 대조군으로는 arbutin (Alfa Aesar, USA)을 100 μg/mL 농도로 사용하였다.
5. NO 생성 억제능 측정
AM과 AMB의 NO 생성 억제능은 세포 배양액내 NO양을 nitrite (NO 2-)와 nitrate (NO 3-) 형태로 측정하는 Green et al. (1982)의 방법을 이용하여 측정하였다. RAW 264.7 세포를 96 well plate에 well당 5×10 4 cells/well의 농도로 분주하고, 24 h 동안 배양 후 배지를 제거한 다음 1 μg/mL lipopolysaccharide (LPS; Sigma-Aldrich)가 처리된 DMEM 배지에 시료를 3.75, 7.5, 15, 20 μg/mL의 농도별로 처리하여 48 h 동안 배양하였다. 배양된 세포 배양 상층액 100 μL 와 griess reagent (Sigma-Aldrich) 100 μL을 새로운 96 well plate에서 혼합하여 차광된 상태에서 10 min 반응시킨 후 microplate reader를 이용하여 540 nm에서 흡광도를 측정하였다. NO 생성 억제능은 다음의 식에 따라 산출하였으며, LPS 군과 비교하였다.
6. Western blotting
AMB에 대한 B16F10 melanoma 세포 내 MITF, tyrosinase 활성 억제능 및 RAW 264.7 세포 내 COX2 단백질 발현 억제능을 확인하기 위해 Western blotting을 실시하였다. B16F10 melanoma 세포와 RAW 264.7 세포를 1.5×105 cells/well의 농도로 분주하여 24 h 동안 배양한 후 B16F10 melanoma 세포에 100 mM α-MSH와 RAW 264.7 세포에 1 μg/mL LPS이 처리된 DMEM 배지에 각각 B16F10 melanoma 세포에 AMB를 25 μg/mL, RAW 264.7 세포에 AMB를 20 μg/mL의 농도로 처리한 다음 두 세포 모두 동일한 방법으로 48 h 배양한 세포를 수확하여 PBS로 세척 후 radioimmunoprecipitation assay (RIPA) buffer [50 mM Tris-Cl (0.2% Tween 20, pH 7.5), 50 mM sodium chloride (NaCl), 1% NP-40, 0.5% sodium deoxycholate (C24H39NaO4), 0.1% sodium dodecyl sulfate (SDS), protease inhibitor cocktail; Roche, Switzerland]로 첨가하여 세포를 용해한 후 상등액을 회수하였다. 단백질을 변성시키기 위하여 SDS sample buffer [14.4 mM 2-mercaptoethanol, 60 mM Tris (pH 6.8), 25% glycerol, 2% SDS, 0.1% bromophenol blue]를 첨가한 후 sodium dodecyl sulfate-polyacrylamide gel electrophoresis (SDS-PAGE)를 이용하여 단백질을 분자량별로 분리하였다. 분리된 단백질은 100 V의 조건에서 nitrocellulose membrane (Whatman, GE Healthcare Life Sciences, UK)으로 transfer한 다음 membrane에 옮겨진 단백질을 5% skim milk 용액에서 blocking 한 후 1×tris-buffered saline with tween 20 [TBST; 150 mM NaCl, 10 mM Tris-Cl (0.2% Tween 20, pH 7.5)]에 희석한 β-actin primary antibody (1:10,000, Sigma-Aldrich), anti-MITF antibody produced in rabbit (1:3,000, Sigma-Aldrich), antityrosinase antibody produced in mouse (1:3,000, Sigma-Aldrich)를 처리하고 24 h 동안 교반하였다. Secondary antibody는 anti-mouse IgG antibody, anti-rabbit IgG antibody (Santa Cruz Biotechnology, USA)을 사용하여 30 min 교반하였으며, 교반이 완료된 membrane은 TBST로 세척하였다. 세척이 완료된 후 실험용 필름(Konica Minolta, Japan)에서 SuperSignalⓇ West Pico Chemiluminescent Substrate (Pierce, Thermo Fisher Scientific, USA)을 처리하여 필름에 감광을 유도한 다음 암실에서 자동현상기(QX-130II, Konica Minolta)를 이용하여 현상하였다. 현상된 필름상의 단백질양은 ImageJ (National Institutes of Health, USA)를 이용하여 band 농도차이를 비교하였다.
7. 통계처리
본 실험의 연구 결과는 평균±표준편차(mean±standard deviation, M±SD)로 표기하였으며, 통계 처리는 Statistical Package for the Social Sciences (SPSS) window version 17.0 (IBM, USA)을 이용하여 분석하였다. 유의성 검증은 Student’s t -test를 실시하였고, p 값이 0.05 미만일 때 통계적으로 유의한 차이가 있는 것으로 판정하였다. 모든 실험은 동일한 조건하에 독립적으로 3회 이상 실시하여 실험 결과를 얻어 분석하였다.
Results and Discussion
1. 항산화 효과 측정 결과
특정한 혼합물 또는 식물 추출물의 자유 라디칼(free radical)을 측정하여 항산화력을 검증하는 방법으로 DPPH 방법이 널리 사용되고 있으며( Choi et al ., 2003), 본 연구에서도 AM과 AMB의 DPPH 라디칼 소거능을 확인하여 항산화력을 측정하였으며, 결과를 Figure 1에 나타내었다. 본 실험 결과, 양성 대조군으로 사용한 ascorbic acid는 1%의 농도에서 97.2%의 높은 라디칼 소거 활성이 확인되었으며, 0.5% 농도에서 AM 52.7%, AMB 51.7%의 라디칼 소거 활성을 확인하였다. Kim et al . (2007)은 75% 에탄올 황기 추출물에 가수분해 효소로 효소 처리하여 DPPH를 측정하였으며, 두 시료 모두 DPPH 라디칼 소거능의 변화는 동일하다고 보고되고있으며, 본 연구에서도 AM과 AMB의 추출방법에 따른 라디칼 소거 활성의 차이는 나타나지 않는 것으로 확인됨에 따라 본 연구결과와 비슷한 결과를 확인하였다.
2. 미백 효과 측정 결과
1) B16F10 melanoma 세포에 대한 세포 생존율
AM과 AMB가 B16F10 세포에 대한 세포 생존율에 미치는 영향을 확인하기 위하여 B16F10 세포에 3.12, 6.25, 12.5, 25, 50 μg/mL의 농도로 처리한 후 NR assay를 실시하였다( Figure 2). 본 실험 결과, AM은 111.5%, 85.5%, 95.6%, 85.5%, 2.1%로 세포 생존율이 확인되었으며, AMB는 100.0%, 90.7%, 85.8%, 80.8%, 2.1%의 세포 생존율이 확인되었으며, 두 시료 모두 50 μg/mL 농도에서 B16F10 melanoma 세포에 대한 유의한 세포 독성이 확인되었으며, 이러한 결과를 바탕으로 추후 실험에서는 25 μg/mL 이하의 농도로 실험을 진행하였다.
2) 멜라닌 생합성 억제능
AM과 AMB을 3.12, 6.25, 12.5, 25 μg/mL의 농도로 B16F10 melanoma 세포에 처리하여 멜라닌 생합성 억제능을 측정한 결과를 Figure 3에 나타내었다. 본 실험 결과, 멜라닌의 생성을 촉진시키는 것으로 알려진 α-MSH에 의해 멜라닌의 생성을 유의하게 증가시켰으며, 양성 대조군으로 사용된 arbutin을 100 μg/mL 농도로 처리하였을 때( Kim et al ., 2013), 23.4%의 멜라닌 생합성 억제 효과를 나타내었다. 시료가 처리된 25 μg/mL 농도에서 AM은 23.0%, AMB는 42.5%의 높은 멜라닌 생합성 억제효과가 확인되었으며, 특히 AMB는 3.12 μg/mL의 저농도에서 arbutin과 유사한 억제 효과가 확인되었다. 이와 같은 결과를 통해 AM보다 생물전환된 AMB에서 멜라닌 생합성 억제능이 우수한 것으로 판단된다.
3) MITF, tyrosinase 발현량 변화
위의 실험에서 멜라닌 생합성 억제 효과가 뛰어난AMB의 MITF와 tyrosinase의 단백질 발현량을 확인하기 위하여, B16F10 melanoma 세포에 α-MSH를 처리하여 멜라닌의 발현을 활성화시키고, 25 μg/mL 농도의 AMB를 처리한 후 Western blotting을 이용하여 MITF, tyrosinase 단백질 활성 억제 효과를 측정하였다( Figure 4). 본 실험 결과, AMB에 의해 MITF의 활성이 37.0% 감소되는 것이 확인되었으나, tyrosinase 억제 효과는 나타나지 않는 것으로 확인되었다. Joo et al. (2015)의 선행 연구에서는 황기 추출물이 tyrosinase related protein 1 (TRP1), tyrosinase related protein 2 (TRP2), MITF, tyrosinase의 유의한 감소 효과를 확인하였으며, Kim et al. (2011)은 황기 약침액이 tyrosinase 활성을 통계적으로 유의하게 억제한다고 보고함에 따라, tyrosinase 활성 억제 효과는 본 연구와는 다소 차이가 있으나, MITF의 활성 억제 효과는 본 연구와 비슷한 연구 결과가 확인되었다. 이와 같은 연구를 통하여 AMB가 MITF의 활성 억제로 인한 미백 효과가 있을 것으로 사료된다.
3. 항염증 효과 측정 결과
1) RAW 264.7 세포에 대한 세포 생존율
AM과 AMB가 RAW 264.7세포에 대한 세포 생존율에 미치는 영향을 확인하기 위하여 RAW 264.7세포에 3.12, 6.25, 12.5, 25, 50 μg/mL의 농도로 처리한 후 NR assay를 실시하였다( Figure 5). 본 실험 결과, AM은 84.0%, 80.8%, 78.8%, 69.6%, 41.4%로 세포 생존율이 확인되었으며, AMB는 84.5%, 80.9%, 99.0%, 58.8%, 40.0%의 세포 생존율이 확인되었다. 또한, 50 μg/mL 농도에서 두 시료 모두 RAW 264.7세포에 대한 유의한 독성이 확인되었으며, 25 μg/mL 농도에서도 AMB의 독성이 확인되었다. 이러한 결과를 바탕으로 추후 실험에서는 20 μg/mL 이하의 농도로 실험을 진행하였다.
2) RAW 264.7 세포에 대한 NO 생성 억제능
AM과 AMB가 염증 반응의 중요한 인자로 알려진 NO 생성억제 효과에 대하여 확인하기 위하여 RAW 264.7 세포에 염증 매개 물질인 LPS를 처리하여 세포 내 NO 생성을 유도한 다음 AM과 AMB를 처리하여 NO 생성 억제능을 측정하였다( Figure 6). 본 실험 결과, 모든 농도에서 농도 의존적인 NO 생성 억제효과가 확인되었으며, 특히 20 μg/mL 농도에서 AM과 AMB는 77.9%, 84.4%의 유의한 억제 효과를 확인하였고, AMB는 3.75 μg/mL의 저농도에서도 38.7%의 높은 NO 생성 억제 효과를 나타내었다. Mou et al . (2011)의 연구에서 황기 추출물이 NO생성 억제에 중요한 작용을 하는 것으로 보고됨과 같이 AM과 AMB는 NO생성 억제에 중요한 작용을 하는 것으로 사료되며, NO 생성 억제를 통한 면역기능조절과 다양한 피부 염증 반응을 효과적으로 억제하는 효과적인 물질로서의 활용 가능성이 있을 것으로 사료된다.
3) RAW 264.7 세포에 COX2 발현 억제능
위의 실험에서 NO 생성 억제 효과가 뛰어난 AMB에 대하여 RAW 264.7 세포에 염증 매개 물질인 1 μg/mL LPS를 처리하여, 염증을 유도한 후 20 μg/mL AMB를 처리하여 염증성 단백질인 COX2 발현 억제 효과를 Western blotting을 통하여 확인하였다( Figure 7). 본 실험 결과, AMB는 COX2 발현 감소에 큰 영향을 주지 않는 것으로 확인되었다. 이에 따라 AMB는 COX2외의 다른 경로에 의하여 항염증 효과가 나타나는 것으로 사료된다.
Conclusion
본 연구에서는 70% 에탄올로 추출한 황기 에탄올 추출물(AM)과 효소 처리를 통한 황기 생물전환 추출물(AMB)을 이용하여 항산화 활성 및 미백, 항염증 효과를 가진 기능성 화장품 소재로서의 생리활성 효과를 알아보고자 하였다. 본 연구결과, AM과 AMB의 DPPH 라디칼 소거능은 비슷한 활성 효과를 나타냄을 확인하였다. B16F10, RAW 264.7 세포에 대해 AM과 AMB의 세포 생존율을 측정한 결과, B16F10 세포에서는 두 시료 모두 50 μg/mL 농도에서 유의한 세포 독성이 확인되어 추후 실험에서는 25 μg/mL의 농도부터 실험을 진행하였다. RAW 264.7 세포의 경우 25, 50 μg/mL 농도에서 유의한 세포 독성이 확인되어 추후 실험에서는 20 μg/mL 농도부터 실험을 진행하였다. 미백 활성 효과를 확인하기 위하여 멜라닌 생합성 억제능을 측정한 결과, AMB를 25 μg/mL 농도로 처리하였을 때 양성 대조군인 arbutin보다 높은 멜라닌 생합성 억제효과가 확인되었고, 멜라닌 생합성 증가와 관련 있는 MITF 효소를 AMB가 효과적으로 활성 억제함에 따라 미백 효과를 확인하였다. AM과 AMB의 항염증 효과를 확인하기 위하여 RAW 264.7 세포에 대한 NO 생성 저해 효과를 확인하였으며, 모든 농도에서 농도 의존적인 NO 생성 억제 효과가 확인되었고, 특히 AMB는 20 μg/mL의 농도에서 84.4%의 높은 NO 생성 억제효과를 확인하였다. 하지만 염증 과정 중 형성되는 COX2 발현억제와는 큰 영향을 주지 않는 것으로 확인됨에 따라 생체의 염증 반응에 관련이 있다고 알려진 염증성 사이토카인 활성 억제효과에 대한 추가적인 연구가 필요할 것으로 사료된다. 이와 같은 결과를 통하여 AM과 AMB의 항산화 활성, 미백 효과 및 항염증 효과를 가진 기능성 화장품 소재로서의 활용 가능성과 생물전환된 AMB가 다양한 생리활성을 증진시켜 추출물의 유용성과 효과성을 향상시킨 생물전환 화장품 소재로서의 활용 가능성을 확인하였다.
Figure 1.
DPPH radical scavenging activity of AM and AMB.
Free radical scavenging activity was carried out so as to measure anti-oxidant activities of AM and AMB. Moreover, ascorbic acid was used as comparative material (positive control). In the result, it was verified that free radical scavenging activity of AM was higher than that of AMB. With regard to the value, a M±SD is shown. Three independent experiments were performed. DPPH, 2,2-diphenyl-1- picrylhydrazyl; AM, Astragalus membranaceus ethanol extracts; AMB, Astragalus membranaceus bioconversion extracts; Control, untreated group; M±SD, mean±standard deviation.
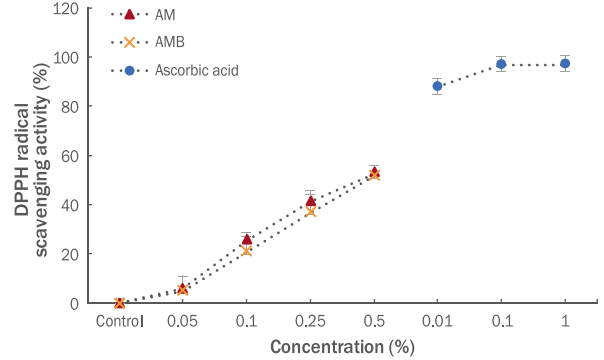
Figure 2.
Cytotoxicity in B16F10 cells.
The cytotoxicity of AM and AMB was measured in B16F10 melanoma cells, and significant cytotoxicity was confirmed in the concentration of 50 μg/mL. With regard to the value, a M±SD was shown. Three independent experiments were performed ( ***p<0.001). The results were compared between control group and experimental group. AM, Astragalus membranaceus ethanol extracts; AMB, Astragalus membranaceus bioconversion extracts; Control, untreated group; M±SD, mean±standard deviation.

Figure 3.
Ability of AM and AMB to suppress melanin synthesis in B16F10 cells.
B16F10 melanoma cells were treated with 100 nM α-MSH. AM and AMB capacity to inhibit melanin synthesis was measured. Arbutin (100 μg/mL) was used as positive control group and the results were compared between α-MSH group and experimental group. Results, Significant at all concentrations of AMB. With regard to the value, a M±SD was shown. Three independent experiments were performed and statistical significance was shown (* p<0.05; **p<0.01). AM, Astragalus membranaceus ethanol extracts; AMB, Astragalus membranaceus bioconversion extracts; Control, untreated group; α-MSH, α-melanocytestimulating hormone; M±SD, mean±standard deviation.
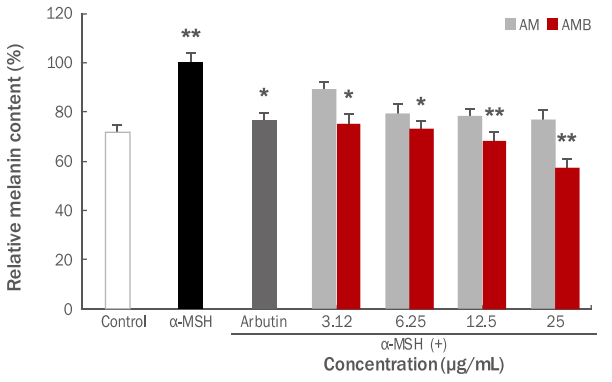
Figure 4.
Inhibitory effects of AMB on MITF and tyrosinase activation in B16F10 melanoma cells.
(A) Image (B) Graph. In order to check the whitening effects of AMB, B16F10 melanoma cells were treated with α-MSH. And an inhibitory effects of AMB on MITF, tyrosinase activities were measured by using western blotting. The results were compared between α-MSH group and experimental group and in MITF, significant inhibitory effects were checked. With regard to the value, a M±SD was shown. Three independent experiments were performed (**p<0.01). AMB, Astragalus membranaceus bioconversion extracts; α-MSH, α-melanocytestimulating hormone; MITF, melanogenesis associated transcription factor; M±SD, mean±standard deviation.
Figure 5.
Cytotoxicity in RAW 264.7 cells.
The cytotoxicity of AM and AMB was measured in RAW 264.7 cells. The results were compared between control group and experimental group, and significant cytotoxicity was confirmed at the concentrations of 25 μg/mL and 50 μg/mL. With regard to the value, a M±SD was shown. Three independent experiments were performed (* p<0.05; ***p<0.001). AM, Astragalus membranaceus ethanol extracts; AMB, Astragalus membranaceus bioconversion extracts; Control, untreated group; M±SD, mean±standard deviation.
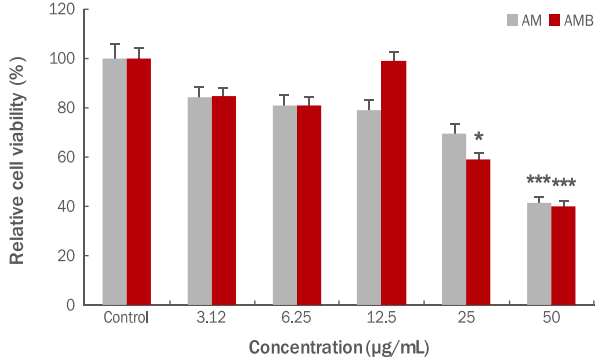
Figure 6.
Inhibition of NO production in RAW 264.7 cells treated with AM and AMB.
Activity was induced by treating RAW cells with LPS, and then inhibitory effects on NO production were measured by treating it with AMB. The results were compared between LPS group and experimental group, and an inhibitory effects on NO production were checked in all concentrations of AMB. With regard to the value, a M±SD was shown. Three independent experiments were performed and statistical significance was shown (* p<0.05; **p<0.01; ***p<0.001). AM, Astragalus membranaceus ethanol extracts; AMB, Astragalus membranaceus bioconversion extracts; NO, nitric oxide; Control, untreated group; LPS, lipopolysaccharide; M±SD, mean±standard deviation.

Figure 7.
Inhibitory effects of AMB on the activation of COX2 by LPS in RAW 264.7 cells.
In order to check the anti-inflammatory effects of AMB, RAW 264.7 cells were treated with LPS, and inhibitory effects on COX2 activity were measured by using western blotting. The results were compared between LPS group and experimental group and COX2 activity was increased. (A) A variation of COX2 protein expression due to AMB was shown. (B) COX2 protein expression due to AMB was graphed. With regard to the value, a M±SD was shown. Three independent experiments were performed and statistical significance was not shown. AMB, Astragalus membranaceus bioconversion extracts; LPS, lipopolysaccharide; COX2, cyclooxygenase 2; M±SD, mean±standard deviation.

References
Bang KH, Huh MK, Cho JH. Genetic diversity and discrimination of Astragalus membranaceus Bunge and A. membranaceus var. mogholicus using RAPD markers. Journal of Physiology & Pathology in Korean Medicine 18: 825-829. 2004.
Blois MS. Antioxidant determinations by the use of a stable free radical. Nature 181: 1199-1200. 1958.   Choi Y, Kim M, Shin JJ, Park JM, Lee J. The antioxidant activities of the some commercial teas. Journal of the Korean Society of Food Science and Nutrition 32: 723-727. 2003.   Green LC, Wagner DA, Glogowski J, Skipper PL, Wishnok JS, Tannenbaum SR. Analysis of nitrate, nitrite, and [15N] nitrate in biological fluids. Analytical Biochemistry 126: 131-138. 1982.   Ha MJ, You SH. Bioactive characteristics of extracts of Opuntia humifusa fruit as functional cosmetic ingredients. Asian Journal of Beauty and Cosmetology 14: 463-472. 2016.   Han DO, Kim GH, Choi YB, Shim I, Lee HJ, Lee YG, Kim JH, Chang GT, Hahm DH. Healing effects of Astragali Radix extracts on experimental open wounds in rats. Journal of Physiology & Pathology in Korean Medicine 19: 92-97. 2005.
Han HS, Kim SY, Lim DJ, Whang WK. Development of whitening cosmetic ingredients from Cudrania tricuspidata stem extract. Asian Journal of Beauty and Cosmetology 14: 317-328. 2016.   Joo DH, Yoo DH, Lee SY, Lee JY. Whitening effect of Astragalus membranceus Bunge water extract and development of cosmeceutical. Jounal of the Korean Society of Cosmetology 21: 888-894. 2015.
Jung TK, Kim MJ, Lim KR, Yoon KS. Moisturizing and antioxidation effect of Astragalus membranaceus root extract. Journal of the Society of Cosmetic Scientists of Korea 32: 193-200. 2006.
Kang SA, Oh MS, Kim DR, Kang JU, Kim WN, Park EH, Chang MS, Park SK. Compositions of Astragali Radix and Angelicae Radix by DPPH radical scavenging activity. The Korea Journal of Herbology 21: 17-24. 2006.
Kim EJ, Moon JS, Choe TB. Inhibition of tyrosinase by Bioconversioned Morus alba extract. Asian Journal of Beauty and Cosmetology 11: 845-854. 2013.
Kim EJ, Yang KS. Effect of Astragali Radix on low density lipoprotein oxidation. Yakhak Hoeji 45: 529-535. 2001.
Kim JH, Jung TY, Lee BH, Lee YK, Kim JS, Lee KM, Lim SC. Effects of Astragali Radix herbal acupuncture extracts on the collagenase activity and procollagen synthesis in HS68 human fibroblasts and tyrosinase activity. The Acupuncture 28: 13-20. 2011.
Kim MJ, Lim KR, Jung TK, Yoon KS. Anti-aging effect of Astragalus membranaceus root extract. Journal of the Society of Cosmetic Scientists of Korea 33: 33-40. 2007.
Lee JY, Park HY, Yeom MH, Kim DH, Kim HK. The protective effects of Astragali Radix against UV induced cellular damage in human keratinocytes. Korean Journal of Pharmacognosy 39: 300-304. 2008.
Lim HW, Cho NY, Yoon MY, Cha SB, Kim KW, Park YM, Lee JY, Lee JH, Kim CJ, Sim SS. Effects of citrus essential oils on melanin production in B16 melanoma cells. Yakhak Hoeji 47: 25-30. 2003.
Ma XQ, Shi Q, Duan JA, Dong TT, Tsim KW. Chemical analysis of Radix Astragali (Huangqi) in China: a comparison with its adulterants and seasonal variations. Journal of Agricultural and Food Chemistry 50: 4861-4866. 2002.   McKenna DJ, Hughes K, Jones K. Astragalus. Alternative Therapies in Health and Medicine 8: 34-40. 2002.
Mou JC, Lee SN, Kim MG, Kim MH, Kim HJ, Jo HJ, Leem KH. Effects of Astragali Radix extracts on the elastase activity and DPPH and NO scavenging activities. The Korea Journal of Herbology 26: 59-63. 2011.
Ryu M, Kim EH, Chun M, Kang S, Shim B, Yu YB, Jeong G, Lee JS. Astragali Radix elicits anti-inflammation via activation of MKP-1, concomitant with attenuation of p38 and Erk. Journal of Ethnopharmacology 115: 184-193. 2008.   Seo DM, Choi DY, Lee JD. Effects of Astragalus membranaceus on angiogenesis. The Acupuncture 24: 113-123. 2007.
Yu HA, Kim CD. Applicability of Lindera obtusiloba flower extracts as cosmetic ingredients. Asian Journal of Beauty and Cosmetology 15: 132-144. 2017.  
|
|